L’insuffisance cardiaque (IC) est l’une des principales causes de décès et d’invalidité dans le monde, affectant des millions de personnes et imposant un fardeau énorme aux systèmes de santé. La maladie survient lorsque le cœur ne peut plus pomper le sang efficacement, laissant les patients essoufflés, fatigués et exposés à un risque de complications potentiellement mortelles.
Pendant des décennies, les scientifiques se sont concentrés sur l’étude des cardiomyocytes, les cellules musculaires du cœur responsables du pompage du sang, pensant qu’ils étaient les principaux moteurs de la maladie. Mais de nouvelles recherches remettent en question cette vision de longue date en montrant qu’un autre groupe de cellules, souvent négligé, joue un rôle central dans la progression de l’IC.
Une étude publiée dans Nature Recherche cardiovasculairerévèle comment un type spécialisé de fibroblastes cardiaques (cellules qui fournissent traditionnellement un soutien structurel) peut activement aggraver l’IC.
Une équipe de recherche dirigée par le professeur Shinsuke Yuasa du Département de médecine cardiovasculaire, de dentisterie et de sciences pharmaceutiques de l’Université d’Okayama, au Japon, avec le Dr Jin Komuro de l’Université de Tokyo, au Japon, a découvert que ces fibroblastes utilisent une voie de signalisation connue sous le nom d’axe MYC-CXCL1-CXCR2 pour favoriser des changements nocifs dans le cœur.
« Nous avons été surpris de découvrir que les fibroblastes, que l’on pensait être des acteurs de soutien au cœur, peuvent en réalité être à l’origine de l’aggravation de l’IC », a déclaré le professeur Yuasa. « Ils envoient des signaux qui perturbent le travail normal des cellules musculaires, réduisant ainsi la capacité du cœur à pomper efficacement. »
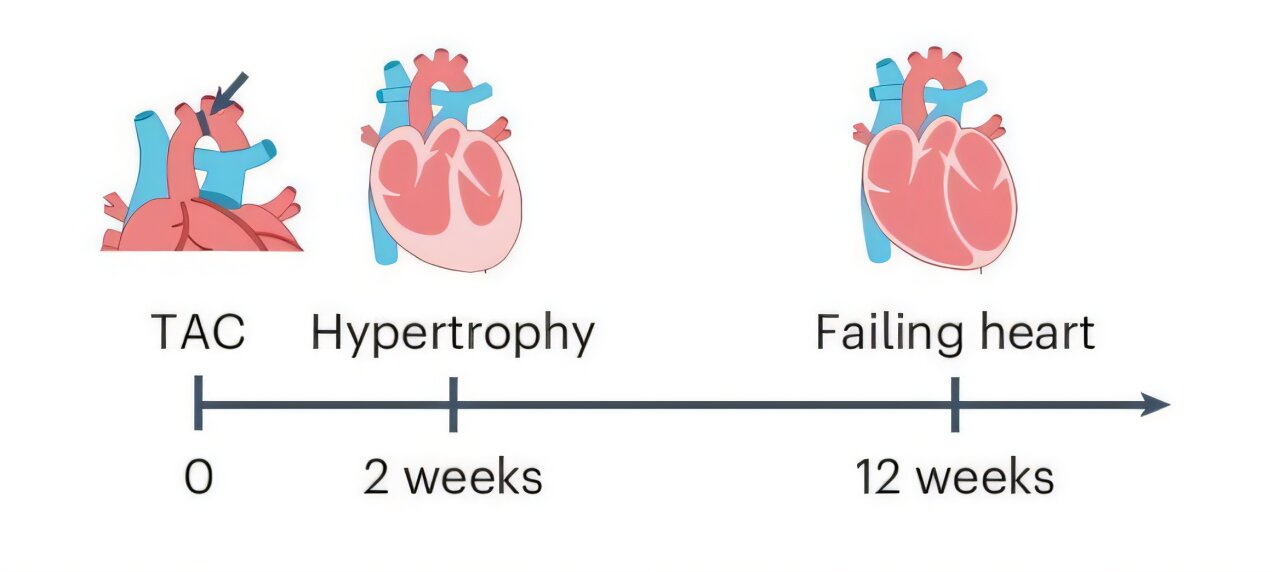
Pour découvrir ce mécanisme, l’équipe a étudié à la fois des échantillons de patients et des modèles expérimentaux d’IC.
En examinant les fibroblastes cardiaques au niveau moléculaire, les chercheurs ont identifié une population de fibroblastes unique aux « cœurs défaillants » dans des modèles de souris qui expriment le gène Myc. Ces fibroblastes libèrent une chimiokine (molécule de signalisation), CXCL1, qui détruit la fonction des cardiomyocytes via son récepteur complémentaire CXCR2, exprimé sur les cardiomyocytes.
En termes plus simples, les fibroblastes communiquent avec d’autres cellules à l’aide de signaux chimiques, mais en cas d’IC, cette communication devient nocive. La voie de signalisation et les signaux chimiques qui en résultent affaiblissent les cellules du muscle cardiaque, entraînant la progression de la maladie.
Les chercheurs ont découvert que le blocage de cette voie chez des modèles murins améliorait la fonction cardiaque, ce qui suggère que les fibroblastes pourraient être une cible potentielle pour de nouvelles stratégies thérapeutiques.
Les chercheurs ont ensuite examiné si ces résultats étaient applicables à l’IC humaine. Ils ont utilisé des échantillons de biopsie cardiaque provenant de patients atteints d’IC et de patients en bonne santé ayant servi de contrôle. Ils ont découvert que MYC et CXCL1 étaient exprimés en quantités élevées dans les fibroblastes cardiaques de patients atteints d’IC, ce qui suggère que l’axe MYC-CXCL1-CXCR2 est responsable du dysfonctionnement cardiaque dans le cœur humain.
« Cette découverte ouvre de nouvelles possibilités de traitement », a déclaré le professeur Yuasa. « En cas d’IC sévère, la transplantation reste souvent la seule option. En ciblant les fibroblastes et leurs voies de signalisation, nous pourrons peut-être développer des thérapies qui ralentiront la progression de la maladie et offriront plus de choix aux patients », explique-t-il.
Ces résultats sont importants car ils remettent en question l’idée selon laquelle la recherche sur l’IC devrait se concentrer principalement sur les cardiomyocytes. En montrant que les fibroblastes contribuent également au dysfonctionnement cardiaque, l’étude élargit les opportunités de découverte de médicaments.
« Cette recherche est une extension de nos études de longue date sur l’IC », a souligné le professeur Yuasa. « Nous espérons que nos recherches inspireront une approche plus multiforme, dans laquelle les thérapies s’adresseront non seulement aux cellules musculaires, mais également aux cellules de soutien qui façonnent la maladie. »
Cette nouvelle perspective est particulièrement précieuse étant donné les options limitées actuellement disponibles pour les patients atteints d’IC sévère. Les médicaments peuvent aider à gérer les symptômes, mais pour beaucoup, une greffe reste le seul espoir.
En identifiant les fibroblastes comme facteur causal clé, les scientifiques pourraient être en mesure de développer des médicaments ciblant la voie de signalisation utilisée pour endommager le cœur, offrant ainsi une approche plus directe pour arrêter la progression de la maladie.
Les chercheurs soulignent que même si les résultats sont prometteurs, des travaux supplémentaires sont nécessaires pour les traduire en traitements cliniques. Les études futures se concentreront sur le développement de traitements sûrs capables de bloquer la signalisation des fibroblastes chez l’homme et sur la question de savoir si ces traitements peuvent améliorer les résultats chez les patients atteints de la forme la moins avancée de la maladie.
Dans l’ensemble, en découvrant l’influence inexplorée des fibroblastes, cette étude remodèle notre compréhension de l’IC et met en évidence une nouvelle voie prometteuse pour la gestion des maladies cardiaques.