Selon une nouvelle recherche publiée dans Recherche antivirale.
Le HSV-1 provoque des plaies autour de la bouche, communément appelées boutons de fièvre ou boutons de fièvre. La plupart des gens sont infectés par le HSV-1 pendant l’enfance, et entre 50 % et 90 % des personnes dans le monde sont atteintes du HSV-1. Après l’infection initiale, le HSV-1 reste dans l’organisme et peut se réactiver tout au long de la vie d’une personne. Bien que les infections à HSV-1 soient généralement bénignes, elles peuvent être graves, voire mortelles, pour les personnes dont le système immunitaire est affaibli. Il est essentiel de trouver de nouveaux antiviraux plus efficaces contre cette maladie courante.
Les chercheurs se sont concentrés sur une enzyme appelée peptidyl-prolyl cis-trans isomérase NIMA-interacting 1, ou Pin1, qui régule la stabilité, la fonction et la structure cellulaire des protéines. Lorsque cette enzyme est dérégulée, elle peut jouer un rôle dans diverses pathologies, notamment l’obésité, le cancer, l’insuffisance cardiaque, etc. On sait que les virus, tels que le cytomégalovirus (CMV) et le SRAS-CoV-2, affectent Pin1, et des inhibiteurs de Pin1 ont été développés pour réduire l’impact de ces virus.
Étant donné que les cellules infectées par le HSV surexpriment Pin1, les chercheurs ont voulu savoir si les inhibiteurs de Pin1 pouvaient également être utilisés pour traiter le HSV-1. « Cette étude a révélé que le facteur hôte Pin1 est une cible thérapeutique cruciale pour la prolifération du HSV-1. Les inhibiteurs de Pin1 suppriment puissamment la réplication du HSV-1 à de faibles concentrations », a déclaré Takemasa Sakaguchi, professeur à l’École supérieure des sciences biomédicales et de la santé de l’Université d’Hiroshima, au Japon.
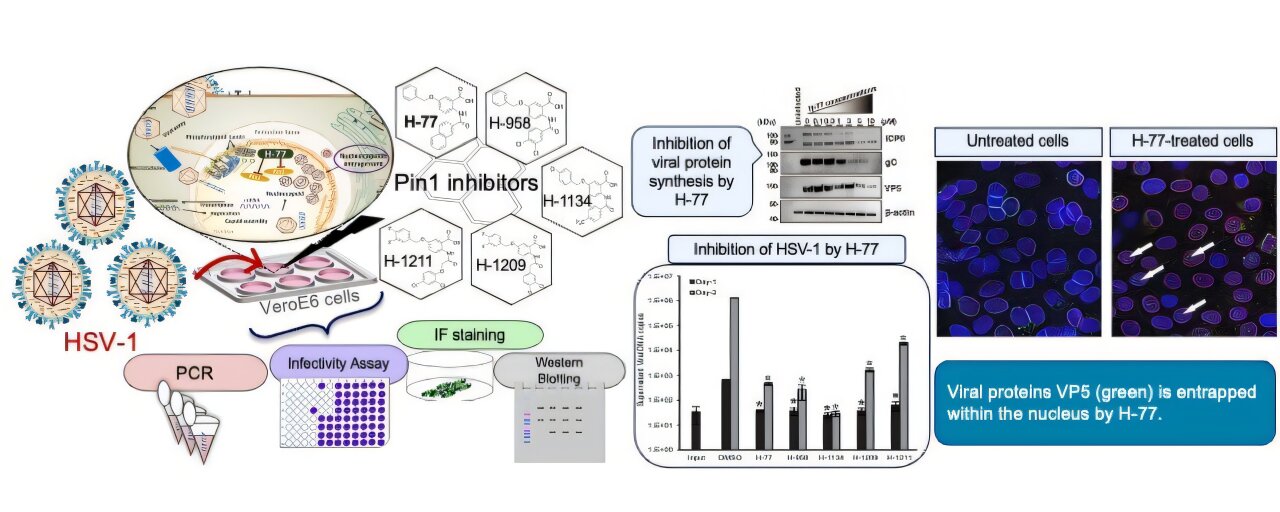
Lors de tests en laboratoire, l’inhibiteur Pin1 H-77 et les quatre inhibiteurs Pin1 nouvellement développés ont réussi à arrêter la réplication du HSV-1. Les cellules VeroE6, dérivées du rein d’un singe vert d’Afrique et couramment utilisées dans la recherche en virologie, ont été infectées par le HSV-1 et cultivées en présence de différentes quantités d’un inhibiteur Pin1. À mesure que la quantité d’inhibiteur augmentait, les effets du HSV-1 sur les cellules devenaient moins prononcés et disparaissaient complètement à 1 µM. Ils ont également constaté que toutes les particules virales libérées par les cellules traitées n’étaient pas infectieuses.
La découverte la plus importante de cette étude est la manière dont les inhibiteurs de Pin1 affectent les structures cellulaires pour empêcher le virus de s’échapper. Pour ce faire, ils stabilisent la structure de la membrane nucléaire, emprisonnant physiquement le virus dans le noyau cellulaire.
« La lame nucléaire fonctionne initialement comme une « barrière » lorsque les nucléocapsides des virus descendants, qui se répliquent dans le noyau, bourgeonnent à partir de la membrane nucléaire. Pin1 surexprimé par le virus supprime cette barrière.
« Cependant, grâce à l’action de l’inhibiteur Pin1 H-77, cette barrière est plutôt renforcée, formant une couche de lame épaisse et robuste. Cela démontre que H-77 transforme la lame nucléaire en un « mur défensif imprenable », bloquant physiquement la fuite des virus du noyau de la cellule », a déclaré Sakaguchi.
À l’avenir, les chercheurs continueront d’évaluer l’efficacité des inhibiteurs Pin1 pour traiter le HSV-1. Ils rechercheront également comment les inhibiteurs de Pin1 pourraient être utilisés pour traiter d’autres virus.
« L’objectif ultime pour l’avenir est de viser l’application clinique des inhibiteurs Pin1 en tant que » thérapies dirigées par l’hôte « , qui sont moins susceptibles de provoquer une résistance aux médicaments. Pour y parvenir, nous évaluerons d’abord leur efficacité contre divers virus afin de clarifier la gamme traitable. Simultanément, la recherche visant à optimiser la structure du composé est essentielle pour créer des médicaments plus puissants et plus sélectifs », a déclaré Sakaguchi.