De nouvelles recherches ont identifié l’enzyme glutamate déshydrogénase 1 (Glud1) comme une nouvelle cible thérapeutique pour la dystrophie musculaire de Duchenne (DMD). Dans les modèles de souris DMD précliniques, les chercheurs ont démontré que l’inhibition de Glud1 améliore considérablement la force et la coordination musculaire, signalant un déplacement potentiel vers la restauration de la fonction musculaire plutôt que de simplement gérer les symptômes. L’étude révolutionnaire en L’American Journal of Pathology pointe vers une voie prometteuse et réalisable pour traiter le DMD en fonction de l’exploitation du glutamate musculaire, répondant à un besoin cliniquement satisfait.
La dystrophie musculaire comprend un groupe de troubles dégénératifs musculaires génétiques conduisant à un gaspillage musculaire progressif. Le DMD est la forme la plus courante et la plus sévère de dystrophie musculaire, affectant 1 sur 3 500 à 5 000 naissances mâles vivantes dans le monde.
Les défauts sous-jacents du gène de la dystrophine provoquent une perturbation des fibres musculaires et des ondes chroniques de dégénérescence musculaire et de régénération. Il en résulte l’accumulation de cellules inflammatoires, de fibrose et de dysfonctionnement des précurseurs musculaires, entraînant finalement une perte de masse et de fonction musculaire. L’approche thérapeutique du DMD se concentre principalement sur le soulagement des symptômes par traitement avec des glucocorticoïdes.
Le chercheur principal Prof. Massimiliano Mazzone, Ph.D., Laboratoire de l’inflammation et de l’angiogenèse tumorales, VIB-Ku Leuven, Leuven, Belgique, dit, « Nous avons précédemment démontré que l’inhibition pharmacologique et génétique de Glud1 – une enzyme qui convertit les macrophies de la macrophace α-glutarat) et vice versa ( Régénération musculaire améliorée et récupération fonctionnelle dans les modèles de blessures aiguës, d’ischémie et de vieillissement.
« Étant donné l’absence d’un remède définitif pour le DMD et l’efficacité limitée des thérapies actuelles, qui visent principalement à ralentir la progression de la maladie et à améliorer la qualité de vie, nous étions impatients de déterminer si le ciblage Glud1 pourrait offrir de nouvelles idées thérapeutiques spécifiquement pour cette maladie. »
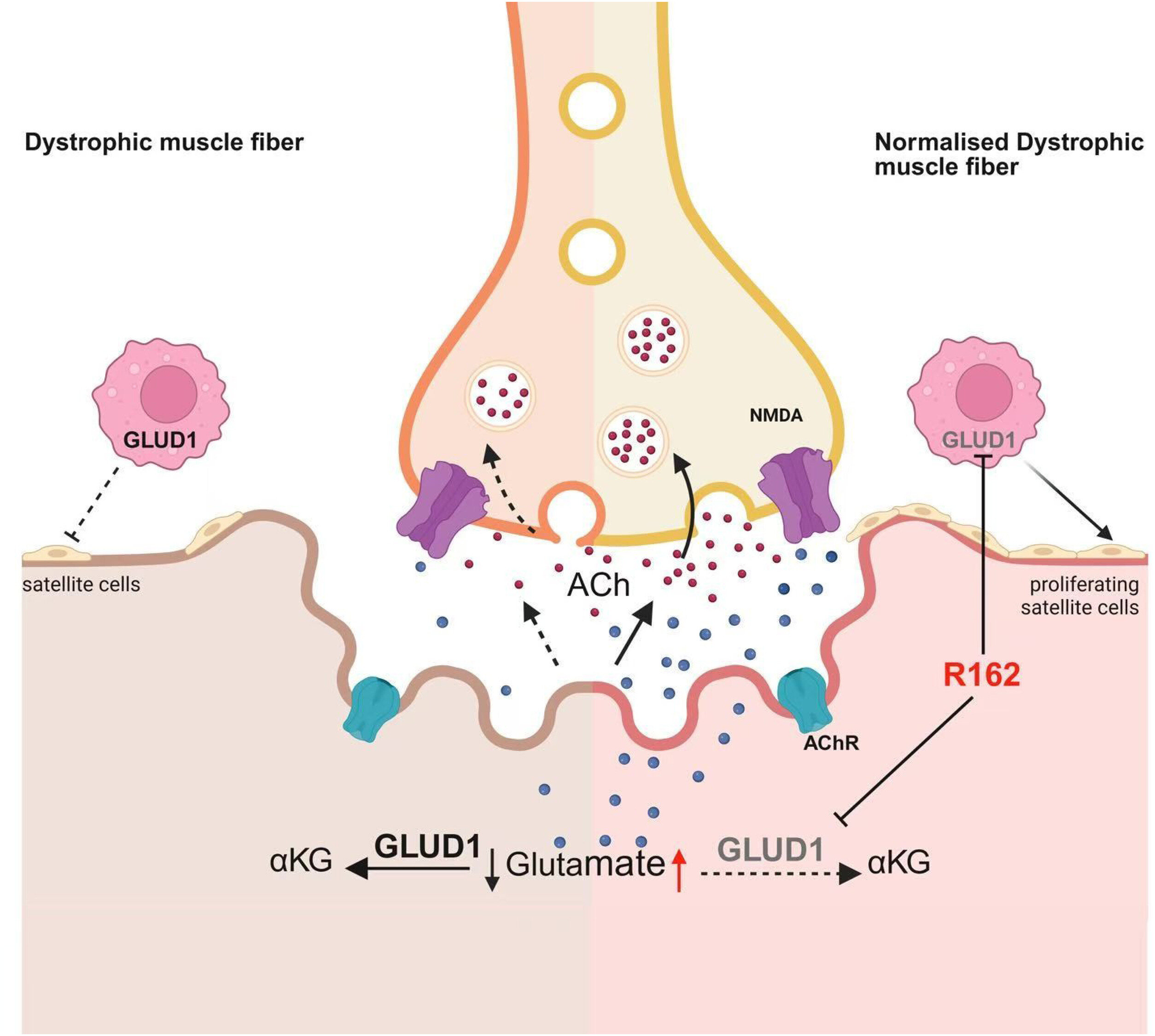
Les chercheurs ont étudié le potentiel thérapeutique de cibler le métabolisme du glutamate dans la DMD en utilisant l’inhibiteur de Glud1 R162. Dans un modèle de souris DMD préclinique (souris MDX), le traitement systémique R162 a considérablement amélioré la force musculaire et la coordination.
L’enquêteur co-dirigé Emanuele Berardi, Ph.D., Laboratoire de l’inflammation et de l’angiogenèse des tumeurs, du VIB-Ku Leuven, et du laboratoire d’ingénierie tissulaire, Ku Leuven, Leuven, Belgique, explique: « Cette récupération fonctionnelle a été liée à des dommages musculaires réduits, à la structure myogénique améliorée de la structure et de la fonction de la fonction de la salite.
« Fait intéressant, alors que l’inhibition de Glud1 dans les macrophages seuls a favorisé l’activation des cellules satellites, il n’était pas suffisant pour restaurer la fonction musculaire, mettant en évidence le rôle essentiel mais non autonome des macrophages dans la régénération musculaire. Nous avons en outre démontré que les macrophages sont nécessaires pour médiation complète de la thérapeutique de R162, en particulier dans le support du NMJ. ».
Le co-investigateur Andreia Pereira-Nunes, Ph.D., Laboratoire d’inflammation tumorale et d’angiogenèse, VIB-KU LEUVEN, LEUVEN, BELGIUM, et Institut de recherche sur les sciences de la santé (ICVS), Braga, le Portugal, ajoute: « Mécaniscain, le traitement de R162 reprogrammé Glutamate Disponibilité, qui à son tour a amélioré la réorganisation morphologique de la NMJ et les niveaux d’acétylcholine restaurés.
Cette étude introduit une nouvelle approche thérapeutique non stéroïdale qui ne cible pas directement le défaut génétique du DMD mais améliore plutôt la fonction neuromusculaire par reprogrammation métabolique. La double action thérapeutique de R162 dans l’amélioration de la fonction et de la neurotransmission des cellules précurseurs musculaires (cellule satellite) offre une approche prometteuse et potentiellement traduisible pour améliorer les résultats des patients, en particulier compte tenu de son efficacité et de sa sécurité chez les souris dystrophiques utilisées pour étudier le DMD.
Co-investigateur Ummi Ammarah, Ph.D. candidat, laboratoire de l’inflammation tumorale et de l’angiogenèse, VIB-ku Leuven, Leuven, Belgique et Molecular Biotechnology Center, University of Turin, Turin, Italie, conclut, «Nos résultats fournissent la première épreuve de concept que les médicaments métaboliques peuvent être utilisés efficacement pour traiter les dystrophies musculaires, offrant une nouvelle stratégie par bypasse fonction. »