Les maladies neurodégénératives, comme la maladie d’Alzheimer et la démence, sont des pathologies qui entraînent une perte progressive des neurones et un déclin des fonctions cérébrales. Des études antérieures ont découvert un lien entre ces maladies et l’accumulation de protéines mal repliées, telles que la protéine tau et l’α-synucléine.
Tau est une protéine présente principalement dans les neurones qui aide généralement à stabiliser les structures qui transportent les nutriments et les molécules dans les neurones, appelées microtubules. L’α-synucléine, quant à elle, est une petite protéine située à l’extrémité des neurones (c’est-à-dire les pré-synapses), qui aide généralement à réguler la fonction des vésicules synaptiques, de petits sacs qui libèrent des neurotransmetteurs à travers les synapses.
Bien que ces protéines jouent un rôle important dans un cerveau sain, leur agrégation anormale s’est avérée être une caractéristique de plusieurs maladies neurodégénératives. Les processus moléculaires qui provoquent leur accumulation ne sont cependant pas encore entièrement élucidés.
Des chercheurs de l’Université de Washington à Saint-Louis et de l’Université de Californie ont récemment étudié le rôle d’une molécule d’ARN récemment découverte, appelée FAM151B-DT, dans l’agrégation des protéines tau et α-synucléine. Leurs conclusions, publiées dans Psychiatrie Moléculairesuggèrent que cet ARN est un régulateur clé de l’homéostasie des protéines, ou en d’autres termes, qu’il aide à maintenir un équilibre dans la production et la dégradation des protéines dans le cerveau.
« Les maladies neurodégénératives partagent des caractéristiques communes d’agrégation des protéines ainsi que d’autres traits pléiotropiques, notamment des changements dans les schémas transcriptionnels, la neuroinflammation, une perturbation de la signalisation synaptique, un dysfonctionnement mitochondrial, un stress oxydatif et des mécanismes de clairance altérés comme l’autophagie », ont écrit Arun Renganathan, Miguel A. Minaya et leurs collègues dans leur article.
« Cependant, les régulateurs clés de ces traits pléiotropes doivent encore être identifiés. Nous avons utilisé la transcriptomique, la spectrométrie de masse et les analyses biochimiques pour définir le rôle d’un nouvel ARNnc sur la physiopathologie de la protéine tau. »
Un ARN jusqu’alors inconnu impliqué dans l’agrégation des protéines
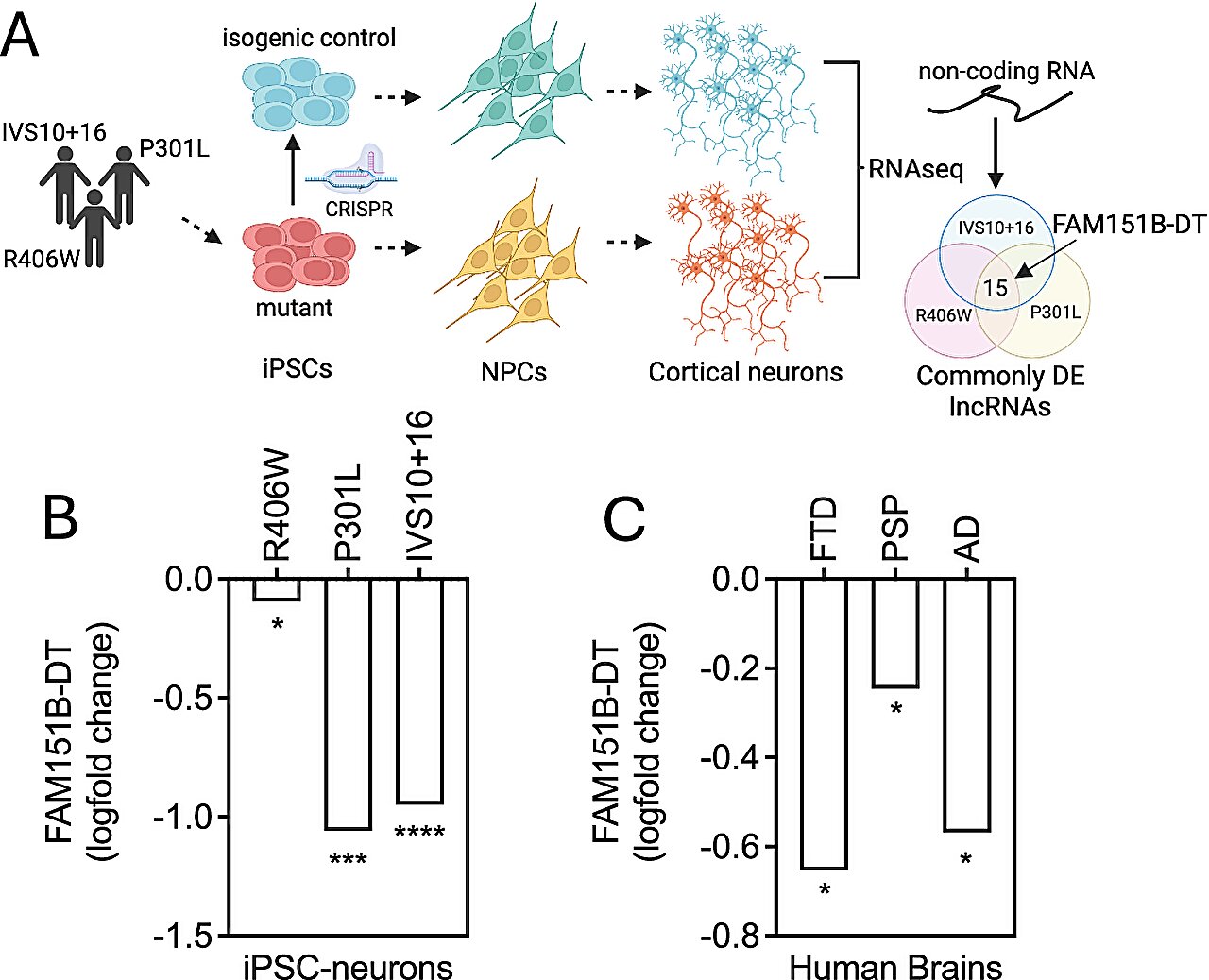
Dans le cadre de leur étude, Renganathan et ses collègues ont examiné des cellules souches et des échantillons de tissus à l’aide d’un large éventail d’outils génétiques et expérimentaux. Plus précisément, ils ont comparé les niveaux de protéine lncRNA dans les tissus cérébraux provenant d’individus ayant reçu un diagnostic de maladie neurodégénérative à ceux de personnes qui ne l’étaient pas.
« Nous avons découvert un long ARN non codant (lncRNA), FAM151B-DT, réduit dans un modèle de cellules souches de démence lobaire frontotemporale avec inclusions de tau (FTLD-tau) et dans le cerveau de patients atteints de FTLD-tau, de paralysie supranucléaire progressive, de maladie d’Alzheimer et de maladie de Parkinson », ont écrit Renganathan et leurs collègues. « Nous montrons que la désactivation de FAM151B-DT in vitro est suffisante pour améliorer l’agrégation de la protéine tau et de l’α-synucléine. »
Les chercheurs ont cultivé des cellules souches en laboratoire, puis ont réduit au silence la protéine qu’ils ont identifiée dans ces cellules. Ils ont notamment constaté que cela augmentait l’agrégation de protéines associées à diverses maladies neurodégénératives.
« Pour commencer à comprendre le mécanisme par lequel FAM151B-DT intervient dans l’agrégation de la protéine tau et contribue à plusieurs maladies neurodégénératives, nous avons caractérisé en profondeur ce nouvel ARNnc et découvert que FAM151B-DT réside dans le cytoplasme où il interagit avec la protéine tau, l’α-synucléine », ont écrit les auteurs. « HSC70 et d’autres protéines impliquées dans l’homéostasie des protéines. Lorsqu’il est inhibé, FAM151B-DT bloque l’autophagie, conduisant à l’accumulation de tau et d’α-synucléine. »
Informer le traitement des maladies neurodégénératives
Dans l’ensemble, les résultats de cette étude récente suggèrent que la molécule d’ARN FAM151B-DT revêt une importance capitale pour l’équilibrage des protéines tau et α-synucléine dans les cellules. Faire taire cette molécule semble provoquer une agrégation indésirable de protéines liée à des lésions neuronales et à l’émergence de maladies neurodégénératives.
Les informations recueillies par Renganathan et leurs collègues pourraient améliorer la compréhension actuelle de diverses maladies neurodégénératives. À l’avenir, la molécule qu’ils ont identifiée pourrait s’avérer être une cible prometteuse pour traiter précocement ces maladies ou traiter certains de leurs symptômes.
« Il est important de noter que nous avons découvert que l’augmentation de l’expression de FAM151B-DT est suffisante pour favoriser la clairance autophagique de la tau phosphorylée et de l’α-synucléine, et pour réduire l’agrégation de la tau et de l’α-synucléine », ont écrit les auteurs. « Dans l’ensemble, ces résultats ouvrent la voie à une exploration plus approfondie du FAM151B-DT en tant que cible moléculaire prometteuse pour plusieurs maladies neurodégénératives. »
Écrit pour vous par notre auteur Ingrid Fadelli, édité par Gaby Clark, et vérifié et révisé par Robert Egan, cet article est le résultat d’un travail humain minutieux. Nous comptons sur des lecteurs comme vous pour maintenir en vie le journalisme scientifique indépendant. Si ce reporting vous intéresse, pensez à faire un don (surtout mensuel). Vous obtiendrez un sans publicité compte en guise de remerciement.