L’un des agents pathogènes infectieux les plus omniprésents de l’humanité est responsable de la maladie auto-immune chronique appelée lupus érythémateux disséminé (lupus), ont découvert les chercheurs de Stanford Medicine et leurs collègues.
Le virus Epstein-Barr (EBV), qui réside silencieusement dans le corps de 19 Américains sur 20, est directement responsable de la réquisition de ce qui commence comme un nombre infime de cellules immunitaires pour devenir des voyous et persuader un bien plus grand nombre de leurs collègues cellules immunitaires de lancer un assaut généralisé sur les tissus du corps, ont montré les scientifiques.
L’ouvrage est publié dans la revue Médecine translationnelle scientifique.
« Il s’agit de la découverte la plus marquante issue de mon laboratoire dans toute ma carrière », a déclaré William Robinson, MD, Ph.D., professeur d’immunologie et de rhumatologie et auteur principal de l’étude. « Nous pensons que cela s’applique à 100 % des cas de lupus. »
L’auteur principal de l’étude est Shady Younis, Ph.D., professeur en immunologie et rhumatologie.
Plusieurs centaines de milliers d’Américains (près d’un million selon certaines estimations) et environ cinq millions dans le monde souffrent de lupus, dans lequel le système immunitaire attaque le contenu des noyaux cellulaires. Cela entraîne des dommages aux organes et aux tissus dans tout le corps – peau, articulations, reins, cœur, nerfs et ailleurs – avec des symptômes variant considérablement selon les individus. Pour des raisons inconnues, neuf patients lupiques sur dix sont des femmes.
Avec un diagnostic et des médicaments appropriés, la plupart des patients atteints de lupus peuvent vivre une vie raisonnablement normale, mais pour environ 5 % d’entre eux, le trouble peut mettre leur vie en danger, a déclaré Robinson, professeur James W. Raitt, MD. Les traitements existants ralentissent la progression de la maladie mais ne la guérissent pas, a-t-il déclaré.
Le virus rencontre le lymphocyte B
Au moment où nous atteignons l’âge adulte, la grande majorité d’entre nous a été infectée par l’EBV. Transmise par la salive, l’infection par l’EBV survient généralement pendant l’enfance, en partageant une cuillère ou en buvant dans le même verre qu’un frère ou une sœur ou un ami, ou peut-être pendant notre adolescence, en échangeant un baiser. L’EBV peut provoquer une mononucléose, « la maladie du baiser », qui commence par une fièvre qui s’atténue mais se transforme en une profonde fatigue qui peut persister pendant des mois.
« Pratiquement, la seule façon de ne pas contracter l’EBV est de vivre dans une bulle », a déclaré Robinson. « Si vous avez vécu une vie normale », les chances sont de près de 20 contre 1 que vous y parveniez.
Une fois que vous avez été infecté par l’EBV, vous ne pouvez pas vous en débarrasser, a déclaré Robinson, même si vous restez ou ne présentez plus de symptômes. L’EBV appartient à une grande famille de virus, dont ceux responsables de la varicelle et de l’herpès, qui peuvent déposer leur matériel génétique dans les noyaux des cellules infectées. Là, le virus sommeille sous une forme latente, se cachant des agents de surveillance du système immunitaire. Cela peut durer aussi longtemps que la cellule dans laquelle il se cache reste en vie ; ou, dans certaines conditions, le virus peut se réactiver et forcer la machinerie réplicative de la cellule infectée à produire une myriade de copies d’elle-même qui se propagent pour infecter d’autres cellules et d’autres personnes.
Parmi les types de cellules dans lesquels l’EBV s’établit de manière permanente figurent les cellules B, des cellules immunitaires qui accomplissent plusieurs tâches importantes après avoir ingéré des fragments d’agents pathogènes microbiens. D’une part, ils peuvent produire des anticorps : des protéines personnalisées qui trouvent et se lient à des protéines ou à d’autres molécules qui stimulent le système immunitaire (les immunologistes les appellent « antigènes ») sur des agents pathogènes microbiens qui ont infecté un individu ou tentent de le faire.
De plus, les lymphocytes B sont ce que les immunologistes appellent des « cellules professionnelles présentatrices d’antigènes » : elles peuvent traiter les antigènes et les afficher à leur surface de manière à encourager d’autres cellules immunitaires à augmenter l’intensité de leur chasse à l’agent pathogène en question. Il s’agit d’un multiplicateur de force substantiel pour déclencher une réponse immunitaire.
Notre corps abrite des centaines de milliards de cellules B qui, au cours de nombreuses divisions cellulaires, développent une énorme diversité d’anticorps. Au total, ces anticorps peuvent se lier à environ 10 à 100 milliards de formes antigéniques différentes. C’est pourquoi nous sommes capables de mettre en place une réponse immunitaire efficace contre tant d’agents pathogènes différents.
Curieusement, environ 20 % des cellules B de notre corps sont autoréactives. Ils ciblent les antigènes appartenant à nos propres tissus, non pas intentionnellement, mais en raison de la manière aléatoire dont se produit la diversité des cellules B : par une réplication bâclée, apparemment conçue par l’évolution pour assurer la diversification. Heureusement, ces cellules B sont généralement dans un état d’inertie stupide et laissent pratiquement nos tissus tranquilles.
Mais parfois, les cellules B autoréactives somnolentes s’activent, visent nos propres tissus et déclenchent l’un des troubles collectivement appelés auto-immunité. Certaines cellules B autoréactives éveillées produisent des anticorps qui se lient aux protéines et à l’ADN à l’intérieur des noyaux de nos cellules. De tels « anticorps antinucléaires » activés – la marque du lupus – déclenchent des dommages aux tissus répartis de manière aléatoire dans tout le corps, car pratiquement toutes les cellules de notre corps ont des noyaux.
La grande majorité des personnes infectées par l’EBV (c’est-à-dire la plupart d’entre nous) n’ont aucune idée qu’elles abritent toujours un virus et ne contractent jamais le lupus. Mais pratiquement toutes les personnes atteintes de lupus sont infectées par l’EBV, selon des études. Un lien entre l’EBV et le lupus est suspecté depuis longtemps, mais n’a jamais été établi jusqu’à présent.
La cellule B antinucléaire devient désagréable
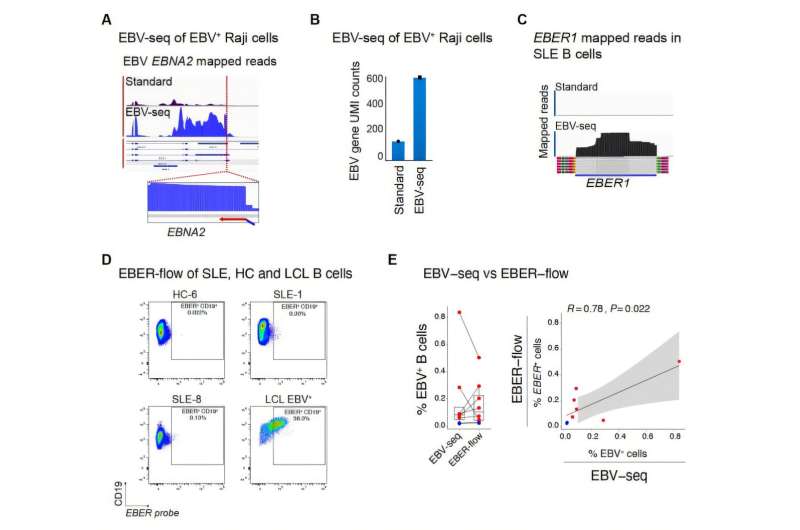
Bien que l’EBV latent soit omniprésent dans le sens où presque tout le monde en est porteur, il ne réside que dans une infime fraction des cellules B d’une personne donnée. En conséquence, jusqu’à la nouvelle étude, il était pratiquement impossible pour les méthodes existantes d’identifier les cellules B infectées et de les distinguer des cellules non infectées. Mais Robinson et ses collègues ont développé un système de séquençage de très haute précision qui leur a permis d’y parvenir. Ils ont découvert que moins de 1 cellule B sur 10 000 d’un individu typique infecté par l’EBV mais par ailleurs en bonne santé héberge un génome viral EBV dormant.
En utilisant leur nouvelle technologie d’identification des cellules B infectées par l’EBV ainsi que des expériences bioinformatiques et de culture cellulaire, les chercheurs ont découvert comment un si petit nombre de cellules infectées peut provoquer une puissante attaque immunitaire sur nos propres tissus. Chez les patients atteints de lupus, la fraction de cellules B infectées par l’EBV s’élève à environ 1 sur 400, soit une différence de 25 fois.
On sait que l’EBV latent, malgré son inactivité quasi totale, pousse néanmoins occasionnellement le lymphocyte B dans lequel il dort pour produire une seule protéine virale, EBNA2. Les chercheurs ont montré que cette protéine agit comme un interrupteur moléculaire – dans le langage des généticiens, un facteur de transcription – activant une batterie de gènes dans le génome du lymphocyte B qui était auparavant au repos. Au moins deux des gènes humains activés par EBNA2 sont des recettes de protéines qui sont elles-mêmes des facteurs de transcription qui activent divers autres gènes humains pro-inflammatoires.
L’effet net de tous ces feux d’artifice génétiques est que le lymphocyte B devient hautement inflammatoire : il revêt son uniforme de « cellule professionnelle présentatrice d’antigène » et commence à stimuler d’autres cellules immunitaires (appelées lymphocytes T auxiliaires) qui partagent une prédilection pour le ciblage des composants cellulaires nucléaires. Ces cellules T auxiliaires recrutent une multitude d’autres cellules B antinucléaires ainsi que des cellules T antinucléaires tueuses, des chiens d’attaque vicieux du système immunitaire.
Lorsque cette milice se renforce, peu importe que l’un des lymphocytes B antinucléaires nouvellement recrutés soit infecté ou non par l’EBV. (La grande majorité d’entre eux ne le sont pas.) S’il y en a suffisamment, le résultat est une crise de lupus.
Qu’est-ce qui vient ensuite ?
Robinson a déclaré qu’il soupçonnait que cette cascade d’activation des cellules B auto-ciblées générée par l’EBV pourrait s’étendre au-delà du lupus à d’autres maladies auto-immunes telles que la sclérose en plaques, la polyarthrite rhumatoïde et la maladie de Crohn, où des indices d’activité EBNA2 initiée par l’EBV ont été observés.
La question à un million de dollars : si environ 95 % d’entre nous se promènent avec l’EBV latent dans nos cellules B, pourquoi certains d’entre nous – mais pas tous – développent-ils une auto-immunité ? Robinson spécule que seules certaines souches d’EBV stimulent la transformation des cellules B infectées en cellules « conductrices » présentatrices d’antigènes qui activent largement un grand nombre de cellules B antinucléaires.
De nombreuses entreprises travaillent sur un vaccin contre l’EBV et des essais cliniques sur un tel vaccin sont en cours. Mais ce vaccin devrait être administré peu de temps après la naissance, a noté Robinson, car de tels vaccins ne peuvent pas débarrasser une personne déjà infectée du virus.