NMNAT2 est une protéine clé nécessaire à l’intégrité des axones dont l’épuisement rapide suite à une lésion axonale déclenche la dégénérescence wallérienne. Le mécanisme moléculaire contrôlant le renouvellement de NMNAT2 dans les neurones n’a pas été entièrement compris. On pense que la dégradation de NMNAT2 est accélérée dans les axones en cas de blessure et que NMNAT2 pourrait avoir des mécanismes de régulation différents dans le soma neuronal et les axones.
Dans une étude publiée en ligne dans Journal de biologie cellulaireune équipe de recherche dirigée par le professeur Fang Yanshan de l’Institut de chimie organique de Shanghai de l’Académie chinoise des sciences a identifié FBXO21 comme la protéine F-box et le facteur clé médiant l’ubiquitination et la dégradation de NMNAT2 dans les neurones, et a découvert que l’inactivation de Fbxo21 dans les neurones du ganglion de la racine dorsale de souris augmente les niveaux de NMNAT2 et retarde considérablement la dégénérescence wallérienne.
Les chercheurs ont d’abord démontré que le taux de renouvellement de la protéine NMNAT2 dans le soma et les axones, ainsi qu’avant et après une blessure, est comparable, ce qui suggère un mécanisme unifié contrôlant la dégradation de NMNAT2.
Ils ont ensuite découvert que l’épuisement rapide de NMNAT2 dans les axones blessés est principalement dû au manque d’approvisionnement en protéine NMNAT2 nouvellement synthétisée à partir du soma. Il a été constaté que FBXO21 régulait la stabilité de NMNAT2 et l’intégrité des axones dans le soma et l’axone, qu’ils soient blessés ou non.
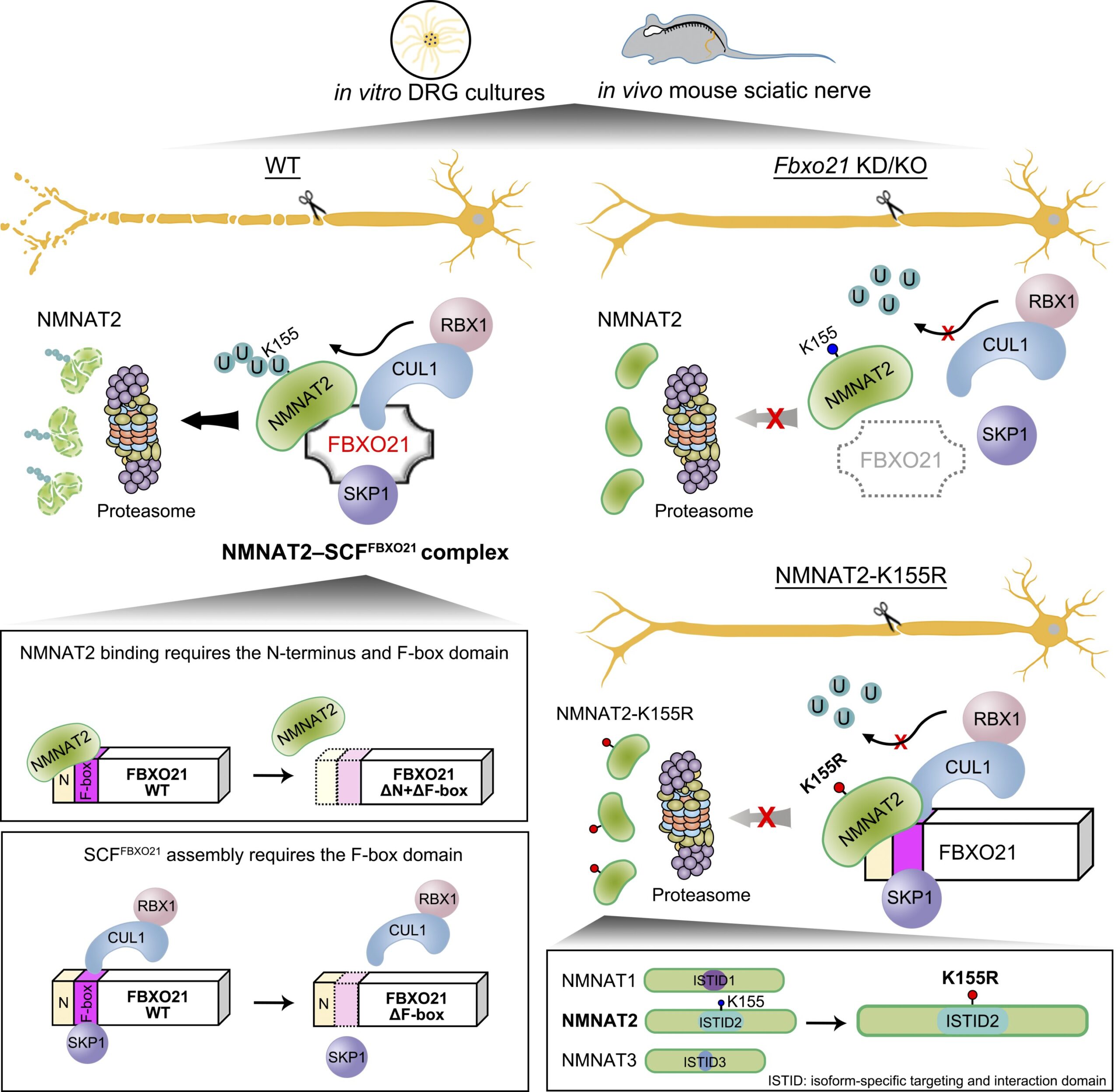
À l’aide de tests d’immunoprécipitation dénaturante et d’ubiquitination in vitro, les chercheurs ont démontré que FBXO21 interagissait avec SKP1, CUL1 et RBX1 pour former un SCF.FBXO21 Complexe E3 ligase qui médie l’ubiquitination de NMNAT2.
Ils ont découvert que SCFFBXO21 NMNAT2 ubiquitiné au niveau de K155 dans le domaine de ciblage et d’interaction spécifique à l’isoforme (ISTID) et la mutation K155R déficiente en ubiquitination ont prolongé de manière significative la demi-vie de NMNAT2 et amélioré considérablement sa protection axonale.
Fait intéressant, les chercheurs ont découvert que l’échange de l’ISTID de NMNAT1 ou NMNAT3 avec celui de NMNAT2 entraînait une dégradation rapide des protéines initialement très stables, tandis que l’introduction de la mutation K155R éliminait cet effet. Ces résultats ont mis en évidence l’ubiquitination de K155 au sein de l’ISTID comme un déterminant évolutif clé de la demi-vie ultra-courte de NMNAT2, révélant la base moléculaire et structurelle de la labilité unique de NMNAT2.
Enfin, les chercheurs ont généré des souris knock-out Fbxo21 et ont révélé que les niveaux de protéine NMNAT2 étaient spécifiquement élevés dans le système nerveux. En utilisant un modèle de lésion du nerf sciatique chez la souris, ils ont démontré que l’inactivation de Fbxo21 retardait considérablement la dégénérescence wallérienne in vivo.
L’étude révèle que FBXO21 joue un rôle clé dans la régulation de la stabilité de NMNAT2 et démontre que la découverte de la protéine FBXO21 déterminant le substrat pour NMNAT2 est particulièrement significative. Il fournit une cible potentielle et une stratégie d’intervention pour améliorer la survie des axones dépendants de NMNAT2 dans les lésions neuronales et les maladies dégénératives.