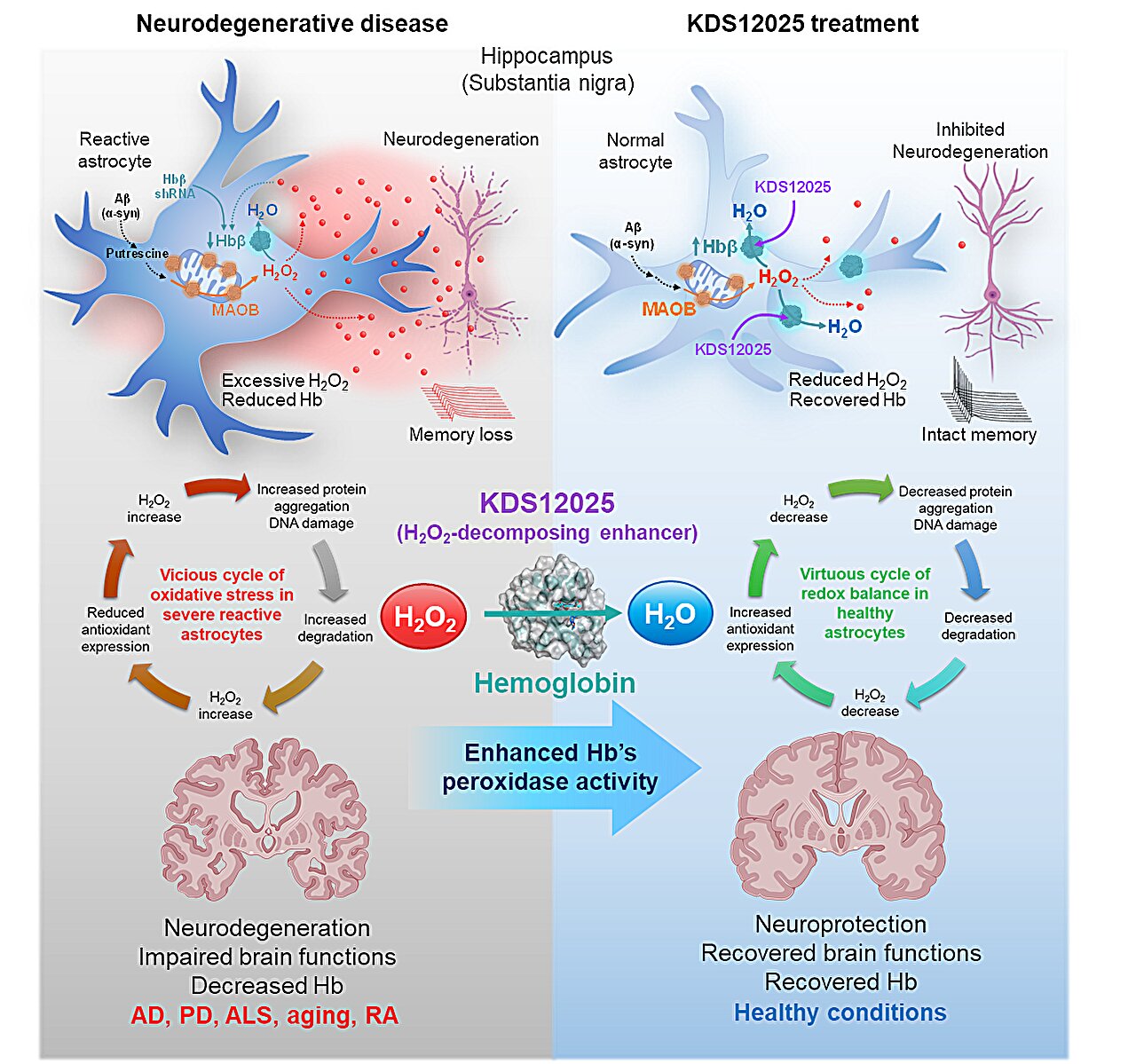
L’hémoglobine, célébrée depuis longtemps pour le transport de l’oxygène dans les globules rouges, s’est maintenant révélée jouer un rôle antioxiant négligé – et potentiellement révolutionnaire dans le cerveau.
Dans les maladies neurodégénératives telles que la sclérose latérale amyotrophique (SLA), la parkinson, la maladie d’Alzheimer et le vieillissement, les cellules cérébrales subissent des dommages incessants des espèces aberrantes (ou excessives) d’oxygène réactif (ROS). Pendant des décennies, les scientifiques ont tenté de neutraliser les ROS avec des médicaments antioxydants, mais la plupart ont échoué: ils ne pouvaient pas pénétrer efficacement le cerveau, étaient instables ou des cellules saines endommagées sans discrimination.
Cette nouvelle étude, dirigée par le réalisateur C. Justin Lee du Center for Cognition and Socialialité au sein de l’Institute for Basic Science (IBS) à Daejeon, en Corée du Sud, a entrepris d’identifier les propres défenses du cerveau contre une forme particulièrement nuisible de ROS – peroxyde d’hydrogène (H (H2O2). L’étude a été publiée dans Transduction du signal et thérapie ciblée.
En utilisant l’imagerie avancée et l’analyse moléculaire, l’équipe a découvert que l’hémoglobine existe dans le nucléole des astrocytes – cellules cérébrales en forme de star critique pour le soutien neuronal – où elle agit comme une «pseudoperoxydase», «décomposant H H2O2 dans l’eau inoffensive.
« La clé était de découvrir le potentiel antioxydant de l’hémoglobine dans le cerveau et de concevoir un composé` `premier en classe » qui pourrait l’améliorer sélectivement. En augmentant un mécanisme de défense naturel plutôt que d’introduire un antioxydant externe, nous avons réalisé une protection solide et détente sur plusieurs modèles de maladies associés au stress oxydatif », a déclaré le premier auteur Dr. Woojin.
L’équipe a développé KDS12025, une petite molécule soluble dans l’eau capable de traverser la barrière hémato-encéphalique. KDS12025 se lie au centre de l’hème de l’hémoglobine et renforce sa capacité à décomposer H2O2 de près de 100 fois, sans perturber sa fonction normale de transport d’oxygène.
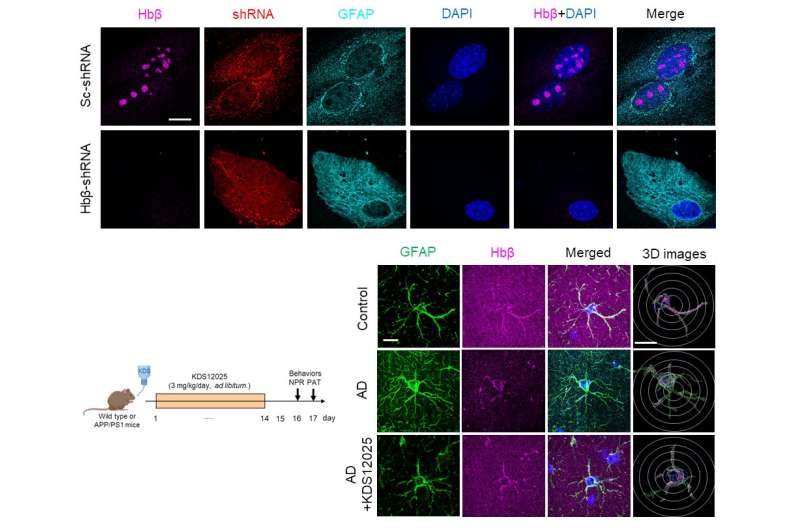
Dans des conditions de maladie dans les astrocytes, KDS12025 a fortement réduit le H nocif H2O2 niveaux. Dans les modèles de souris, l’administration orale par des neurones protégés en eau potable, les astrocytes réactifs calmés et la fonction cérébrale restaurée.
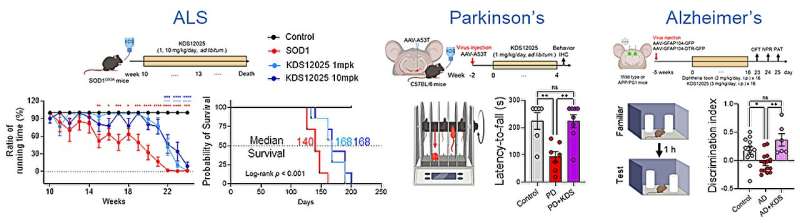
Dans les modèles animaux, l’administration orale par l’eau potable a supprimé la mort neuronale, les astrocytes réactifs normalisés et la fonction cérébrale restaurée. Les souris modèles de la SLA ont montré un début de maladie retardé et ont vécu plus de quatre semaines de plus que les témoins non traités.
Dans les modèles de Parkinson, KDS12025 a restauré la fonction moteur, tandis que dans les modèles d’Alzheimer, il a récupéré les performances de la mémoire. Chez les souris vieillissantes, le traitement a prolongé la durée de vie médiane des deux ans typiques à trois ans. Le médicament a également atténué l’inflammation et les lésions articulaires dans un modèle de polyarthrite rhumatoïde.
L’étude a également révélé une boucle de rétroaction dommageable: excès de H2O2 épuise l’hémoglobine astrocytaire, affaiblissant les défenses antioxydantes naturelles du cerveau et accélérant la dégénérescence. En augmentant les niveaux et l’activité de l’hémoglobine, KDS12025 a inversé cette tendance, réduisant le stress oxydatif, préservant les neurones et maintenant une fonction cérébrale saine.
Aucun traitement précédent n’a ciblé l’hémoglobine astrocytaire en tant que système antioxydant, ni démontré de tels effets protecteurs larges.
« Il s’agit d’un pas en avant majeur dans la lutte contre les maladies neurodégénératives. En améliorant la propre hémoglobine du cerveau pour lutter contre le stress oxydatif, nous ouvrons une toute nouvelle avenue thérapeutique », a déclaré le directeur Lee.
L’équipe prévoit désormais d’étudier davantage les rôles distincts de l’α et de la β-globine dans le cerveau, affinez les dérivés KDS12025 pour une utilisation humaine potentielle et explorez ses applications dans d’autres troubles oxydatifs du stress.
Ce travail transforme l’hémoglobine d’un transporteur d’oxygène familier en un système de défense antioxydant de précision pour le cerveau. Il marque un changement de paradigme potentiel dans la façon dont les scientifiques abordent les maladies neurodégénératives, le déclin lié à l’âge et les conditions auto-immunes.