Les chercheurs de Rutgers en santé ont développé un candidat de médicament antiviral oral pour Covid-19 qui pourrait surmonter les principales limites de Paxlovid, actuellement le traitement oral le plus prescrit.
Comme pour son prédécesseur, le nouveau candidat médicament, JUN13296, cible une protéine virale différente de celle de Paxlovid et fonctionne seule plutôt qu’en combinaison avec un autre médicament appelé ritonavir. Mais Jun13296 bat le premier effort du même laboratoire sur plusieurs mesures cruciales.
« Ce nouveau composé est plus puissant que notre candidat de première génération », a déclaré Jun Wang, auteur senior de l’étude publié dans Communications de la nature et professeur de chimie médicinale à la Ernest Mario School of Pharmacy de l’Université Rutgers.
« Dans les études animales, notre inhibiteur de deuxième génération offre toujours une protection à 90% à un tiers à un tiers de la dose de notre composé initial et le surpasse considérablement pour réduire les charges virales dans les poumons. »
Il aborde également la principale limitation de Paxlovid: effets secondaires induits par l’interaction médicamenteuse.
« La plupart des personnes qui courent un risque élevé de complications induites par les covide prennent déjà des médicaments pour des maladies comme l’hypertension artérielle ou le diabète », a déclaré Wang. « Un grand pourcentage d’entre eux ne peut pas prendre Paxlovid en raison de problèmes d’interaction médicament-médicament. »
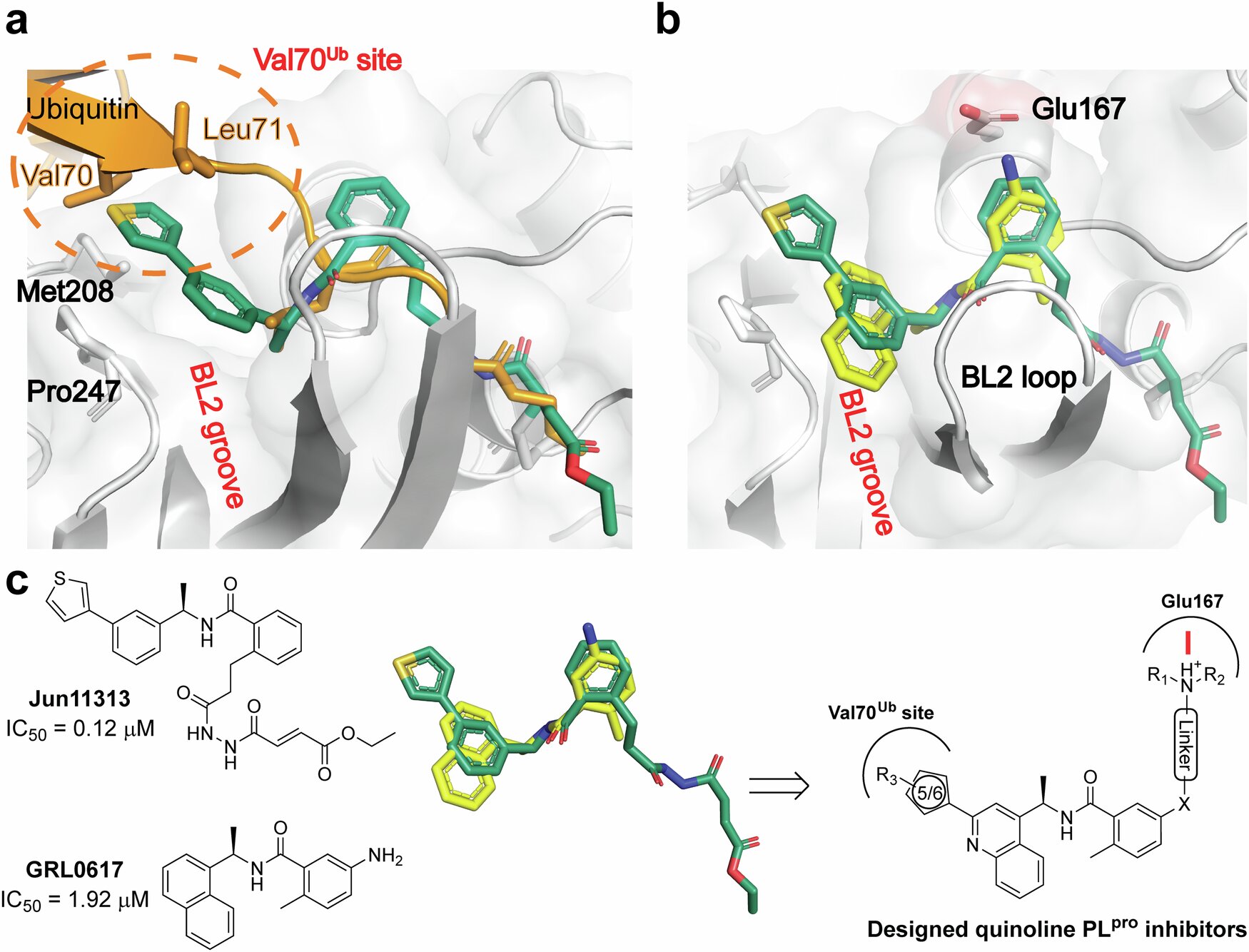
L’équipe de Wang a conçu le nouveau composé pour cibler une structure dans le virus appelé sa protéase de type papaïne (PLPRO) plutôt que la protéase principale ciblée par Paxlovid.
Lors des tests de laboratoire, Jun13296 est resté efficace contre les souches du virus résistantes à Paxlovid.
« Nous avons des données pour confirmer que notre inhibiteur du PLPRO conserve une puissante inhibition contre toutes les variantes que nous avons testées », a déclaré Wang.
Le laboratoire du collaborateur Xufang Deng de l’Oklahoma State University a testé le composé chez des souris infectées par le SARS-COV-2, le virus qui provoque Covid-19. Les taux de survie de cinq jours étaient de 90% pour les souris ayant reçu 13296 juin, 40% pour celles qui ont reçu la même dose faible du composé de première génération en 12682 et 0% pour les souris non traitées.
Le médicament a également considérablement réduit l’inflammation et les niveaux viraux dans les poumons. À 75 milligrammes par kilogramme, JUN13296 a fourni une forte protection contre l’inflammation, tandis que le composé de première génération juin12682 n’a montré qu’une efficacité modérée à cette posologie réduite.
Le plus prometteur est que Jun13296 a fonctionné à des doses comparables ou inférieures à Paxlovid dans des modèles animaux similaires.
« Si vous regardez le modèle animal que les gens ont mené avec Paxlovid, ils doivent traiter les souris avec 150 ou même jusqu’à 300 milligrammes par kilo pour obtenir une efficacité similaire », a déclaré Wang.
L’efficacité à des doses plus faibles aide les patients car il réduit les chances qu’un médicament ait des effets secondaires graves, a déclaré Wang.
Contrairement à Paxlovid, JUN13296 ne montre aucune inhibition des principales enzymes CYP450 de métabolisation médicamenteuse dans les tests de laboratoire, ce qui suggère que cela n’interférerait pas avec d’autres médicaments et n’a pas besoin de co-administrer avec le ritonavir, contournant ainsi les effets latéraux induits par l’interaction médicamenteuse.
Des contributions importantes à cette étude ont été faites par le laboratoire d’Eddy Arnold au Rutgers Center for Advanced Biotechnology and Medicine (CABM), qui a résolu les structures cristallines aux rayons X de PLPRO – critique pour la conception de médicaments basée sur la structure.
Le déplacement du médicament vers des essais humains fait face à des obstacles importants, principalement un financement. Wang a estimé que la prochaine phase coûtera « des dizaines de millions de dollars » au-delà de ce que les laboratoires universitaires peuvent généralement sécuriser.
« Pour aller de l’avant vers des études d’investigation de nouveau médicament et des essais cliniques humains, il peut coûter des dizaines de millions de dollars », a déclaré Wang. « C’est au-delà de ce que nous pouvons faire dans le monde universitaire. »
Son équipe cherche à s’associer à des sociétés pharmaceutiques ou à des organisations à but non lucratif pour faire avancer le composé grâce aux études précliniques requises et éventuellement aux applications de la Food and Drug Administration.
Le développement intervient alors que Covid-19 continue d’évoluer, y compris des variantes résistantes aux traitements existants. Wang a déclaré que le fait d’avoir plusieurs options de traitement reste cruciale pour la préparation pandémique. Même s’il n’est pas immédiatement commercialisé, l’achèvement des essais cliniques à un stade précoce signifierait réduire le temps pour faire approuver le traitement si le SRAS-COV-2 évolue et provoque une autre épidémie ou pandémie.
Les méthodologies développées par l’équipe de recherche sont largement applicables à d’autres maladies infectieuses au-delà de Covid-19. Le laboratoire de Wang est spécialisé dans le développement des antiviraux contre plusieurs virus respiratoires, notamment la grippe et les entérovirus.