Alors que les maladies chroniques du foie se répandent, des chercheurs de Science Tokyo ont développé un organoïde cultivé en laboratoire qui reproduit un foie en régénération, offrant ainsi un nouvel espoir pour de futurs traitements. Le modèle recrée les interactions entre les hépatocytes et les cellules étoilées hépatiques, deux types de cellules impliquées dans la réparation du foie et la fibrose. Il fournit une plate-forme humaine indispensable pour étudier comment les cicatrices hépatiques se développent, comment les cellules communiquent pendant une blessure et pour tester des médicaments qui pourraient arrêter ou même inverser les lésions hépatiques.
Le corps humain possède une extraordinaire capacité de guérison. Cependant, parfois, le système de réparation du corps fait plus de mal que de bien. C’est le cas des maladies hépatiques chroniques, où des blessures répétées déclenchent des cycles de dommages et de réparation qui, au fil du temps, conduisent à une surproduction de matrice extracellulaire (MEC).
À mesure que le tissu hépatique sain est progressivement remplacé par du tissu cicatriciel raide (un processus connu sous le nom de fibrose), il peut évoluer vers une cirrhose, une étape irréversible qui entraîne souvent une insuffisance hépatique. Actuellement, la transplantation hépatique est la seule option thérapeutique pour la cirrhose avancée. Cela met en évidence le besoin urgent de thérapies capables d’arrêter, voire d’inverser la fibrose avant qu’elle ne devienne permanente.
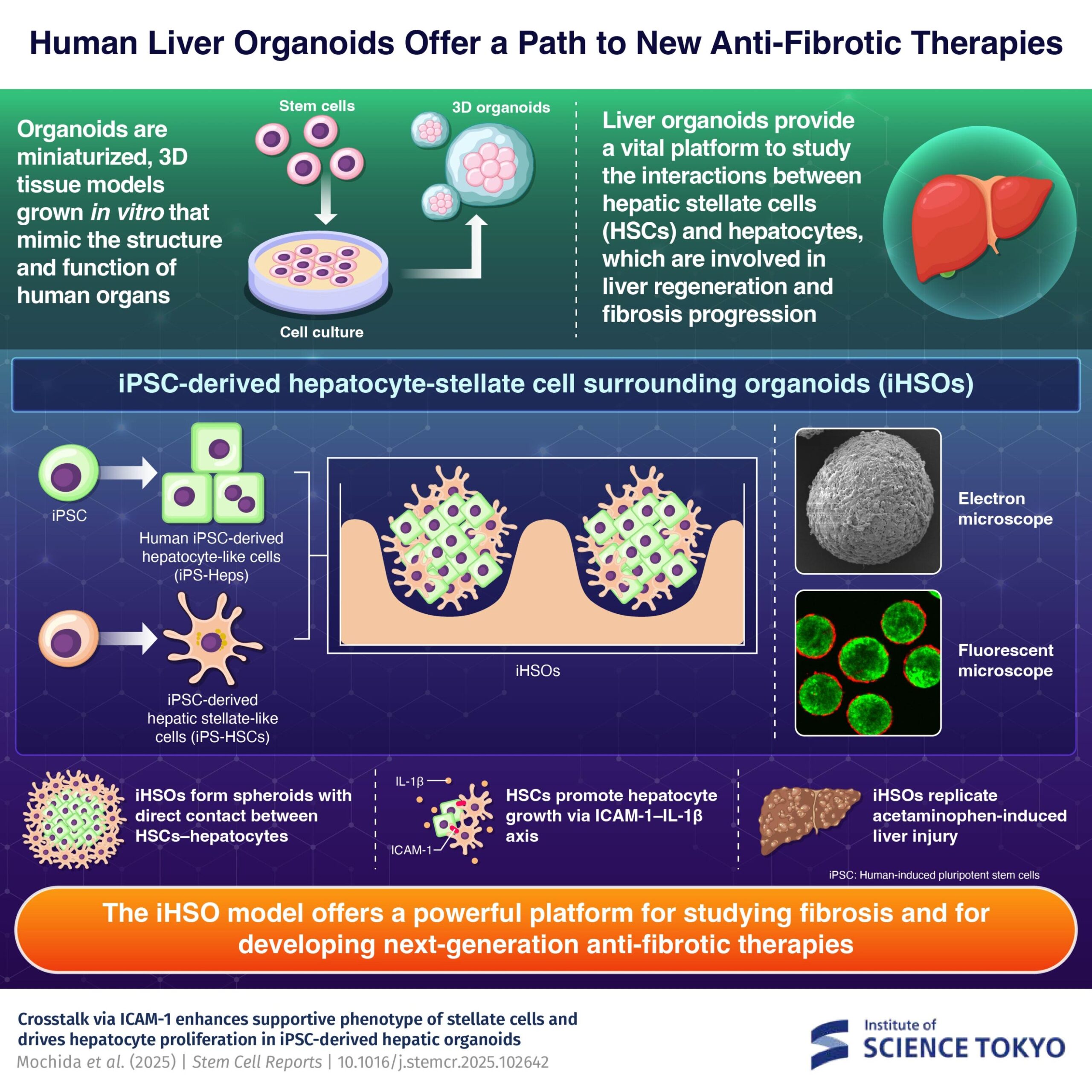
Pour mieux comprendre comment la fibrose se développe, des chercheurs de l’Institut des sciences de Tokyo (Science Tokyo), au Japon, ont créé un nouveau type d’organoïde hépatique humain, un modèle miniature cultivé en laboratoire qui imite la structure et la fonction du tissu hépatique réel. Le modèle, appelé iHSO, qui signifie iPSC-derived hépatocyte-stellate cell entourant organoid, a été conçu pour recréer les interactions entre deux types de cellules clés qui régulent la réparation du foie : les hépatocytes et les cellules étoilées hépatiques (CSH).
L’équipe de recherche était dirigée par le professeur Sei Kakinuma du Département des sciences de laboratoire cliniques et diagnostiques, École supérieure des sciences médicales et dentaires, Science Tokyo, le professeur Yasuhiro Asahina, le professeur adjoint Masato Miyoshi et l’étudiant diplômé M. Tomohiro Mochida du Département de gastroentérologie et d’hépatologie, École supérieure des sciences médicales et dentaires, Science Tokyo, Japon, en collaboration avec l’Université Juntendo. L’étude a été publiée en ligne dans la revue Rapports sur les cellules souches
« Cette étude présente un nouveau système qui aide les chercheurs à mieux comprendre les interactions entre les hépatocytes et les cellules étoilées, ce qui pourrait conduire au développement de nouveaux traitements pour diverses maladies du foie », explique Kakinuma.
Dans un foie sain, les CSH restent au repos et stockent la vitamine A dans de petites gouttelettes lipidiques. Lorsque le foie est lésé, ces cellules reçoivent des signaux provenant d’hépatocytes endommagés – les principales cellules fonctionnelles du foie – ainsi que de cellules immunitaires et endothéliales. En réponse, les CSH s’activent et se transforment en myofibroblastes qui produisent de l’ECM pour réparer les dommages.
Les CSH interagissent également étroitement avec les hépatocytes, formant un système de communication bidirectionnel qui régule à la fois la réparation et la régénération. Les CSH peuvent favoriser la croissance des hépatocytes, tandis que les hépatocytes peuvent influencer l’activation ou la mort des cellules étoilées. Cependant, l’essentiel de cette compréhension provient de modèles animaux, qui n’imitent pas entièrement le comportement des cellules humaines.
Pour combler cette lacune, les chercheurs ont développé un organoïde. À l’aide de cellules souches pluripotentes induites par l’homme (cellules iPS), ils ont généré des cellules de type hépatocytaire (iPS-Heps) et étoilées (iPS-HSC) et les ont co-cultivées en 3D pour former des organoïdes sphériques, avec des cellules étoilées enveloppant les hépatocytes. Leur interaction s’est avérée médiée par ICAM-1, une molécule d’adhésion, et par l’interleukine-1β (IL-1β), une cytokine produite par les CSH. Dans les iHSO, les iPS-HSC présentaient un phénotype calme mais riche en cytokines et soutenaient la prolifération des hépatocytes via l’axe ICAM-1 – IL-1β.
Les iHSO ont également pu modéliser les lésions hépatiques. Lorsqu’ils sont exposés à l’acétaminophène, un médicament pouvant provoquer une toxicité hépatique, les organoïdes ont développé des schémas de lésions similaires à ceux observés dans le foie humain, notamment l’activation des CSH en réponse à des lésions hépatocytaires.
Les maladies chroniques du foie touchent plus de quatre millions d’adultes aux États-Unis, et les cas augmentent au Japon en raison de facteurs tels que la consommation d’alcool et les troubles métaboliques. En fournissant un système réaliste basé sur l’humain pour étudier la fibrose, les iHSO pourraient aider les scientifiques à comprendre comment les cicatrices commencent et à identifier les médicaments qui pourraient les prévenir ou les inverser.
« L’iHSO peut être appliqué à des modèles de lésions hépatiques et devrait contribuer à l’élucidation de la pathogenèse des maladies hépatiques et au développement de nouvelles stratégies thérapeutiques ciblant la fibrose et la régénération du foie », explique Asahina.
À long terme, les résultats de cette étude pourraient conduire à des traitements qui stopperaient, voire répareraient les lésions hépatiques sans nécessiter de greffe.