Avant qu’une chaîne d’acides aminés puisse devenir une protéine active et utile, elle doit être traitée et repliée dans la conformation appropriée. Une grande partie de ce traitement se produit dans le réticulum endoplasmique (ER) de chaque cellule.
Cependant, toutes les perturbations de l’homéostasie des protéines peuvent être très stressantes pour l’ER, et lorsque l’ER est submergée, un système de sécurité appelé la réponse des protéines dépliée (UPR) s’engage à ralentir la synthèse des protéines et à permettre à l’ER de rattraper son retard. Si un ralentissement temporaire de la synthèse des protéines ne suffit pas pour restaurer la fonction ER normale, l’UPR déclenche la mort cellulaire.
Dans de nombreux types de cellules cancéreuses, la réponse UPR est modifiée pour prévenir la mort cellulaire et stimuler la croissance incessante qui caractérise la malignité. Ces changements permettent aux cellules cancéreuses de tolérer le faible environnement d’oxygène et de faible environnement nutritif d’une tumeur et continuent de se multiplier. Les médicaments et les thérapies qui ciblent les parties de la voie UPR pourraient donc être efficaces contre plusieurs types de cancers.
Le professeur Sarah A. Holstein et le Dr Molly E. Muehlebach du Centre médical de l’Université du Nebraska ont examiné en profondeur la façon dont la voie UPR se rapporte aux dommages induits par le cancer dans les os.
Dans leur article de revue publié dans Recherche en osl’équipe a examiné les recherches existantes sur la façon dont la voie UPR est profondément liée à la différenciation des cellules dans le tissu osseux, au maintien et au renouvellement des os, et comment l’infiltration de l’os par les cellules cancéreuses détourne la voie UPR pour provoquer un affaiblissement structurel de l’os.
Cela se produit dans des cancers tels que l’ostéosarcome et le sarcome d’ewing (cancers osseux primaires), ainsi que dans les cancers du sang comme le myélome multiple et les tumeurs solides qui se métastasent en os, comme le cancer du sein ou de la prostate.
Discutant de l’importance de cette recherche, le professeur Holstein dit: « La perturbation du cycle de remodelage peut entraîner une perte osseuse ou une augmentation de la densité osseuse. Cependant, dans les deux cas, l’os est fragile et peut facilement se fracturer.
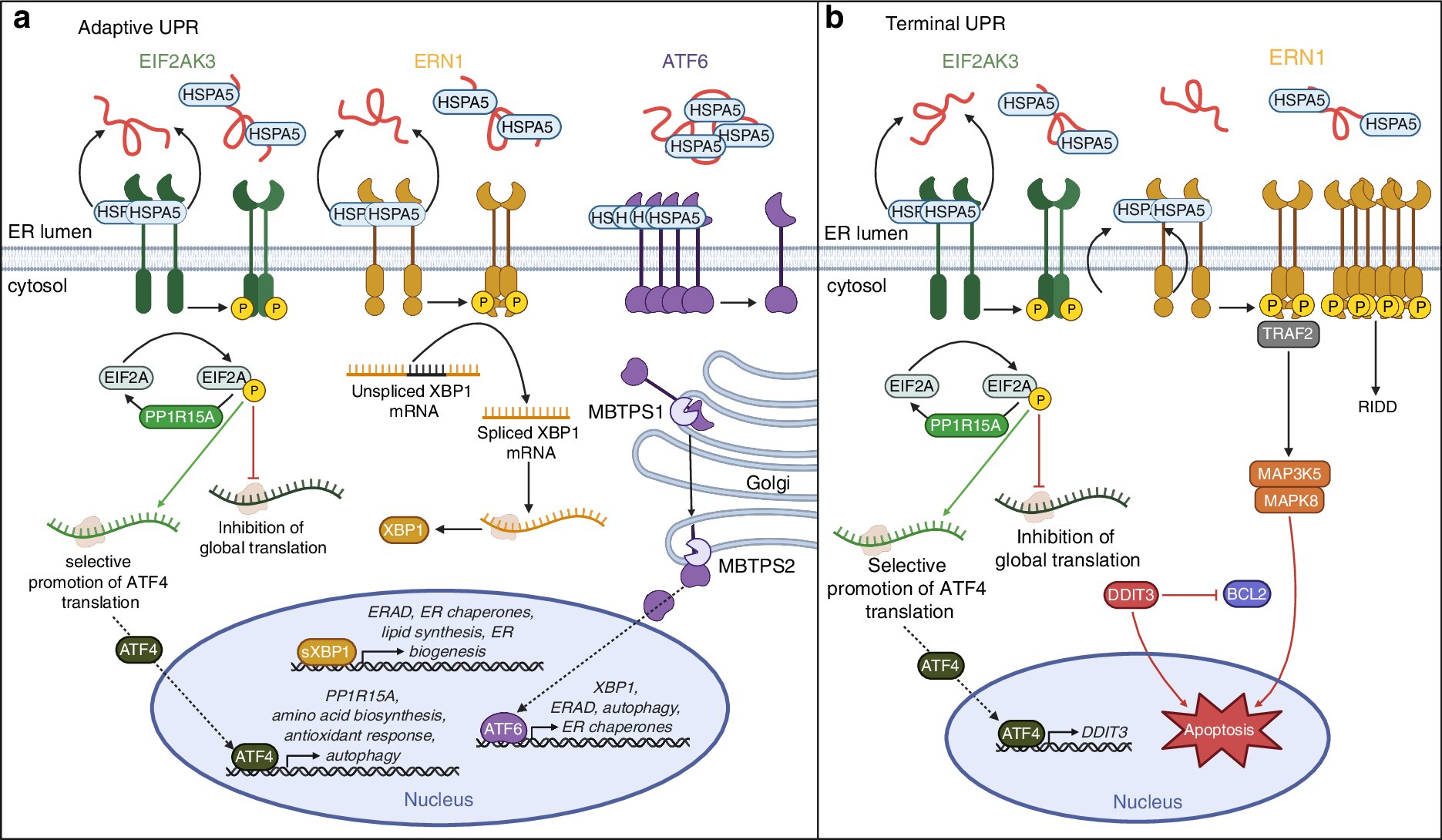
Dans leur article, le professeur Holstein et le Dr Muehlebach regardent d’abord les trois voies UPR primaires – le facteur d’initiation de la traduction eucaryote 2 alpha kinase 3 (eIF2AK3); ER à la signalisation du noyau 1 (ERN1); activer le facteur de transcription 6 (ATF6) et leurs cascades en aval. Ils décrivent ensuite les rôles spécifiques de nombreuses protéines associées à l’UPR dans la différenciation des ostéoblastes (construction osseuse) et des cellules des ostéoclastes (dissolution osseuse) des cellules souches squelettiques.
Les os en bonne santé nécessitent les deux types de cellules pour fonctionner de manière optimale. Cependant, lorsque les cellules cancéreuses envahissent le tissu osseux, elles induisent un dysfonctionnement associé à l’UPR des ostéoclastes, des ostéoblastes, ou les deux, entraînant des os qui sont soit faibles en raison du manque de densité ou de cassure en raison d’une minéralisation excessive. Ces phénomènes sont appelés « événements liés au squelettique » (SRES).
Les classes émergentes de médicaments peuvent réduire le SRES en ciblant des aspects spécifiques de chacune des trois cascades UPR et de leurs protéines en aval. Les mécanismes d’action contre le SRES comprennent:
- Inhibition de eIF2AK3 (par exemple GSK2606414)
- Inhibition de l’ERN1 (par exemple, le sunitinib malate, la toyocamycine)
- Inhibition de la perturbation de la dégradation des protéines associées à l’ER (par exemple, des inhibiteurs du VCP tels que CB-5083)
- Amélioration des protéines chaperon pour augmenter les taux de repliement et soulager le stress ER (par exemple, phénylbutyrate de sodium)
D’autres médicaments émergents à haute affinité pour le tissu osseux induisent l’apoptose médiée par l’EPR dans les cellules malignes par:
- Perturber la synthèse des isoprénoïdes nécessaires au traitement des protéines (par exemple, bisphosphonates acide zolédronique, RAM2061)
- Perturber la dégradation des protéines dépliées (par exemple, oprozomib)
Tous ces médicaments sont à divers stades des essais humains in vitro, animaux ou précoces, et montrent divers degrés de promesse dans l’atténuation des SRES et les tumeurs tuant localisées dans les os. Il reste beaucoup de travail à faire, cependant, pour garantir que ces médicaments de modulation UPR agissent de manière ciblée contre les cellules cancéreuses et ne perturbent pas d’autres fonctions au sein de l’os ou d’autres tissus.
Comme le conclut le professeur Holstein, « en fin de compte, le succès des modulateurs UPR dans le traitement de la maladie osseuse liée au cancer dépendra des agents en développement qui ciblent spécifiquement les cellules osseuses et tumorales tout en minimisant les effets sur les tissus sains ».
Fourni par Cactus Communications