La COVID longue est une maladie clinique hétérogène qui touche des milliers de personnes et peut se manifester de différentes manières. Comprendre pourquoi certaines personnes la développent et d’autres non reste l’un des principaux défis scientifiques.
Une nouvelle étude menée par l’Institut de recherche allemand Trias i Pujol (IGTP) offre une nouvelle perspective : ce qui compte, ce n’est pas seulement les maladies antérieures dont une personne a souffert, mais aussi l’ordre dans lequel elles sont apparues et la manière dont elles interagissent. Cette approche permet d’identifier des profils de risque de COVID long qui n’avaient pas été détectés jusqu’à présent. La recherche a été menée dans le cadre de l’étude COVICAT, coordonnée en collaboration avec l’Institut de Barcelone pour la santé mondiale (ISGlobal).
L’étude, publiée dans Médecine BMC, est basé sur les données de plus de 10 000 participants de la cohorte GCAT (Genomes for Life), qui collecte des informations cliniques et génétiques auprès de la population catalane depuis plus de 15 ans.
À l’aide de ces données, liées au suivi prospectif COVID de l’étude COVICAT lancée en 2020, l’équipe de recherche a reconstruit les trajectoires de santé, c’est-à-dire la séquence temporelle de différentes maladies chroniques, pour analyser comment celles-ci peuvent influencer le développement d’un COVID long.
L’importance de la séquence de la maladie
Jusqu’à présent, la plupart des études se concentraient sur la question de savoir si une personne souffrait ou non d’une maladie antérieure. Ces travaux montrent que la séquence et l’interaction des maladies au fil du temps peuvent également être essentielles pour prédire le risque de développer un long COVID.
« Il ne suffit pas de savoir de quelles maladies une personne est atteinte. L’ordre dans lequel elles apparaissent peut influencer de manière significative le risque, notamment chez les femmes », explique Natàlia Blay, première auteure de l’étude.
Les résultats montrent que la prise en compte de la séquence et de l’interaction des maladies au fil du temps permet une prévision plus précise que de considérer uniquement la présence d’une seule pathologie. Par exemple, les personnes souffrant d’anxiété suivie de dépression courent un risque différent de celles qui souffrent des mêmes conditions dans l’ordre inverse.
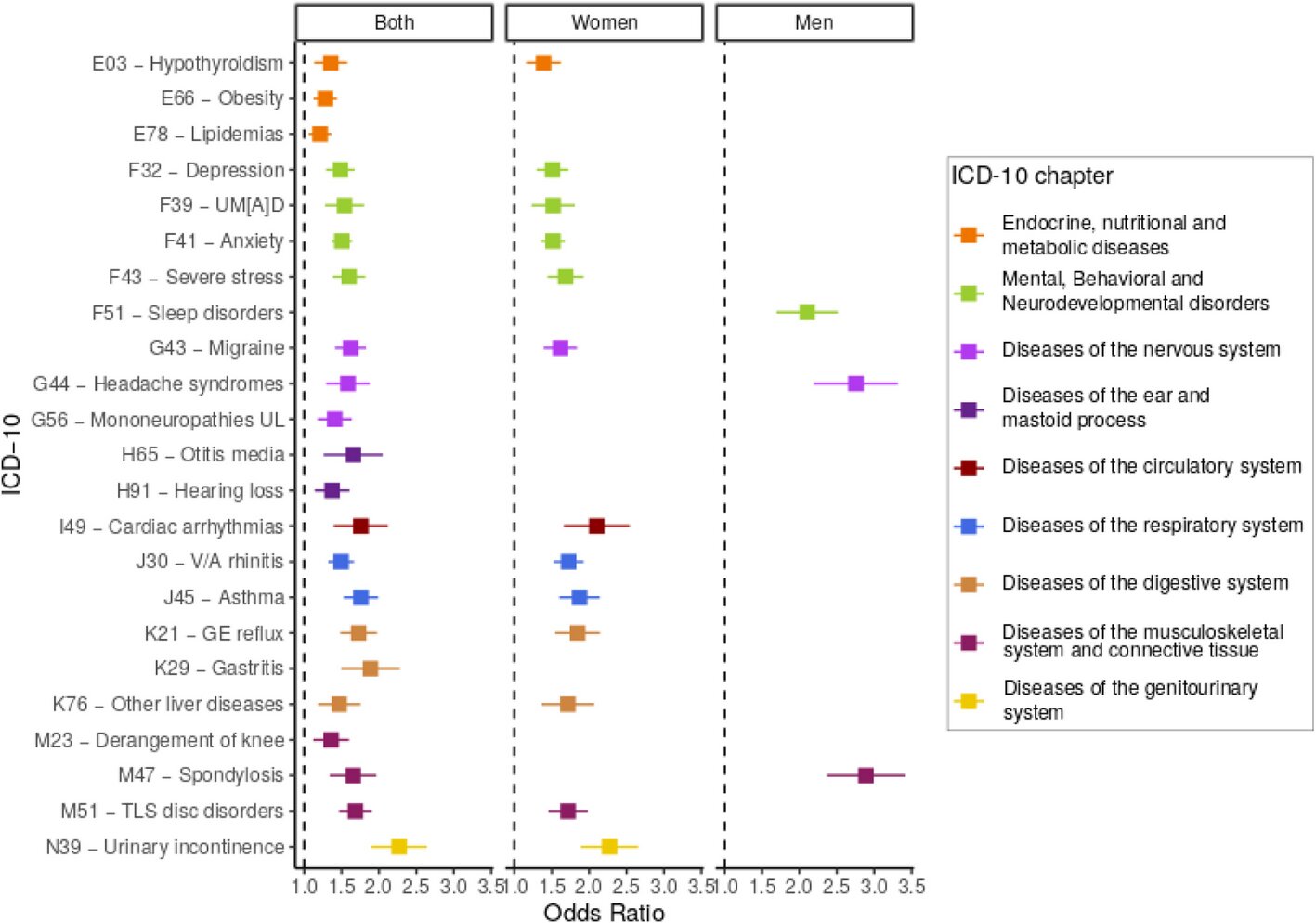
Au total, 162 trajectoires ont été analysées, et 38 étaient associées à un risque significativement plus élevé de COVID long. Les trajectoires les plus fréquentes concernaient des troubles de santé mentale, neurologiques, respiratoires (comme l’asthme) et métaboliques ou digestifs (comme l’hypertension, l’obésité ou le reflux).
L’analyse révèle également que certaines de ces trajectoires de maladie augmentent le risque de COVID long, quelle que soit la gravité de l’infection initiale. Cela indique que tout ne peut pas être expliqué par le type ou l’intensité de la COVID aiguë. Les chercheurs notent qu’à l’avenir, cette approche pourrait bénéficier d’outils d’intelligence artificielle capables de détecter des modèles complexes dans de vastes ensembles de données longitudinales sur la santé, améliorant ainsi la capacité de prédire les risques et d’identifier plus précisément les groupes de population vulnérables.
« Ce travail démontre que le long COVID résulte d’une trajectoire de santé antérieure plutôt que d’un seul facteur. Surtout, il met en évidence que l’étude des trajectoires dans des données longitudinales telles que celles du GCAT a une valeur au-delà du COVID, car elle nous permet d’identifier des modèles de santé de la population qui peuvent aider à prédire d’autres maladies et soutenir une approche de santé publique plus préventive et personnalisée », explique Rafael de Cid, chercheur principal de l’étude et directeur du GCAT à l’IGTP.
Concernant la composante génétique, l’étude ne révèle aucune forte corrélation génétique globale avec le COVID long, bien que des relations modestes aient été trouvées avec des facteurs génétiques liés aux maladies neurologiques et musculo-squelettiques. Ces résultats suggèrent une possible susceptibilité partagée dans certains cas.
L’étude renforce la nécessité de comprendre la santé comme un processus dynamique et cumulatif. L’intégration de la séquence temporelle des maladies aux côtés des informations génétiques peut améliorer la prévision, les soins et la prévention du COVID long et d’autres maladies chroniques.