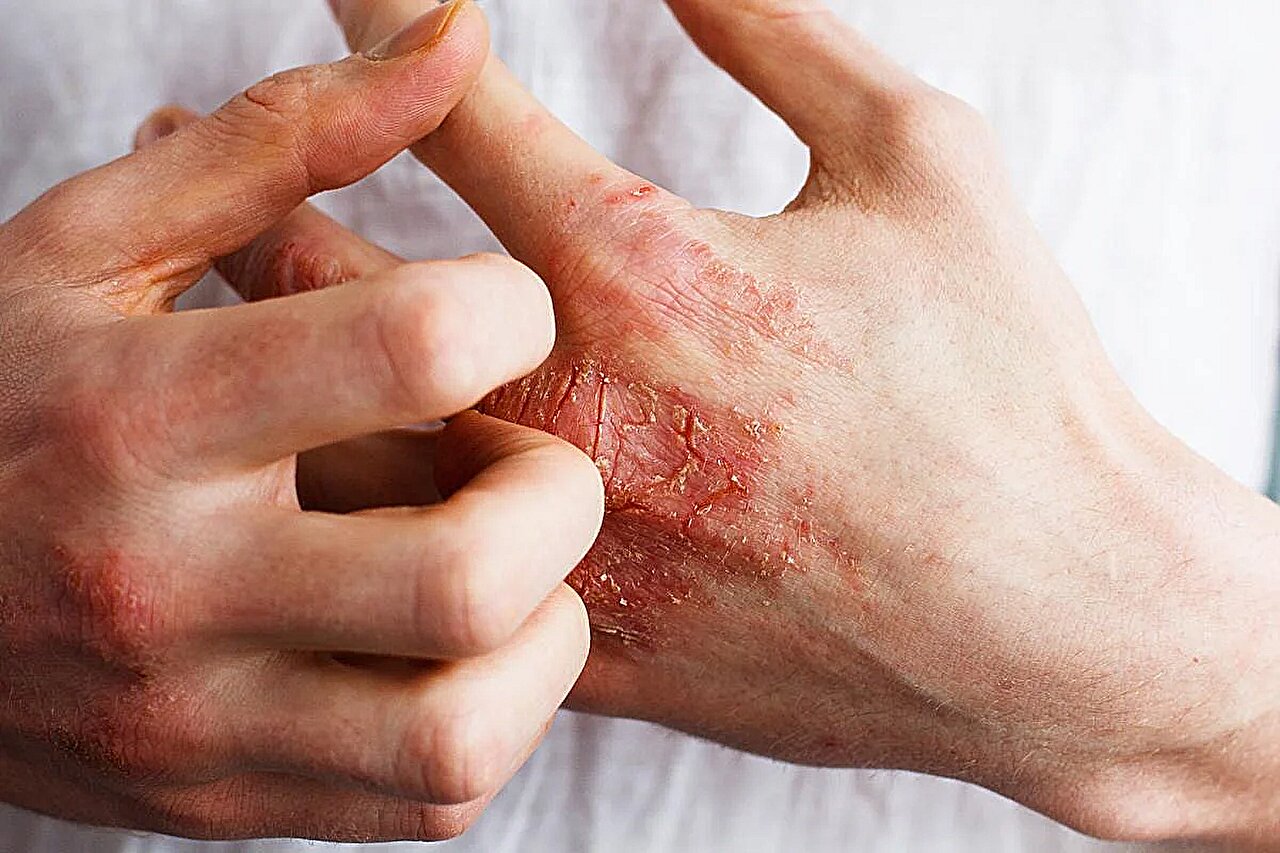
La US Food and Drug Administration (FDA) a signé sur la toute première crème spécifiquement approuvée pour le traitement de l’eczéma chronique des mains (CHE).
Le Che est une condition commune marquée par des rougeurs, des démangeaisons et des fissures sur les mains et les poignets.
Anzupgo (crème delgocitinib) est approuvée pour les adultes atteints de CHE modéré à sévère qui ne peut pas utiliser de stéroïdes topiques ou qui ne leur répondent pas bien.
« L’approbation d’Anzupgo renforce notre engagement à investir dans des affections cutanées difficiles à traiter pour livrer de nouveaux traitements aux patients où le besoin est le plus grand », a déclaré Christophe Bourdon, PDG de Leo Pharma, fabricant d’Anzupgo, dans un communiqué de presse.
Contrairement à la dermatite atopique, qui est la forme la plus courante d’eczéma, le CE est rare et débilitant. Il affecte environ 10% de la population américaine et dure plus de trois mois ou reprend au moins deux fois par an, selon la National Eczema Association.
Anzupgo travaille en bloquant les effets des enzymes JAK, qui déclenchent l’inflammation qui peut lancer une poussée d’eczéma à la main.
La génétique et l’exposition aux irritants et aux allergènes contribuent aux causes de cette forme d’eczéma. Les gens qui sont le plus à risque travaillent dans des industries telles que le nettoyage, la coiffure et les soins de santé, où ils sont plus susceptibles d’entrer en contact avec et de réagir aux produits chimiques.
Des études montrent que la condition peut avoir un bilan spectaculaire sur la qualité de vie d’une personne et le bien-être mental.
Un dermatologue de Détroit a salué l’action de la FDA.
« Au cours de ma carrière de dermatologue, j’ai vu de première main le fardeau important que les démangeaisons et la douleur du CH sont sur les patients, et les défis auxquels ils sont confrontés à vivre », a déclaré le Dr Linda Stein Gold, directeur de la recherche clinique à Henry Ford Health à Détroit, dans un communiqué de presse LEO Pharma US. « Je crois que cette nouvelle option de traitement sera accueillie par les dermatologues qui recherchent des moyens efficaces et sûrs de traiter ces symptômes. »
Des études menant à l’approbation de la FDA ont révélé que les personnes atteintes d’eczéma pour la main qui utilisaient la crème étaient plus susceptibles de s’améliorer que leurs homologues traitées avec un placebo ou une crème factice. La crème ne porte pas le même avertissement en boîte que les autres inhibiteurs topiques et oraux de JAK doivent.
« Nous sommes ravis que la FDA reconnaisse l’impact de l’eczéma chronique modéré à sévère sur les patients », a déclaré Kristin Belleson, PDG et président de la National Eczema Association, dans un communiqué de presse.
« Les personnes vivant avec une maladie cutanée débilitante entre leurs mains trouvent cela extrêmement difficile; cela peut avoir un impact sur leur capacité à travailler, à toucher et à se connecter avec des personnes importantes dans leur vie », a-t-elle ajouté. « L’approbation… donne l’espoir et la promesse de la communauté de l’eczéma et de ceux qui cherchent un soulagement durable des symptômes perturbateurs. »
La crème a déjà été approuvée dans l’Union européenne, le Royaume-Uni, la Suisse et les Émirats arabes unis.