Une équipe de recherche a découvert un nouveau mécanisme qui permet à Mycobacterium tuberculosis (MTB), la bactérie qui provoque la tuberculose (TB), pour échapper aux défenses immunitaires hôtes.
L’étude, publiée dans Rapports cellulairesmontre comment VTT détourne la machinerie d’ubiquitine linéaire de l’hôte pour générer une dégradation du capteur inflammasome NLRP3, contrecarrant ainsi la surveillance immunitaire intracellulaire de l’hôte.
Le VTT continue de menacer les patients en raison de l’émergence et de la propagation de la résistance aux antimicrobiens. Les cellules immunitaires de l’hôte ont des capteurs cytosoliques qui détectent des agents pathogènes envahisseurs et déclenchent des réponses anti-infectieuses. Cependant, la façon dont les agents pathogènes tels que le VTT sapent la surveillance intracellulaire de l’hôte pour provoquer une infection persistante n’est pas entièrement comprise.
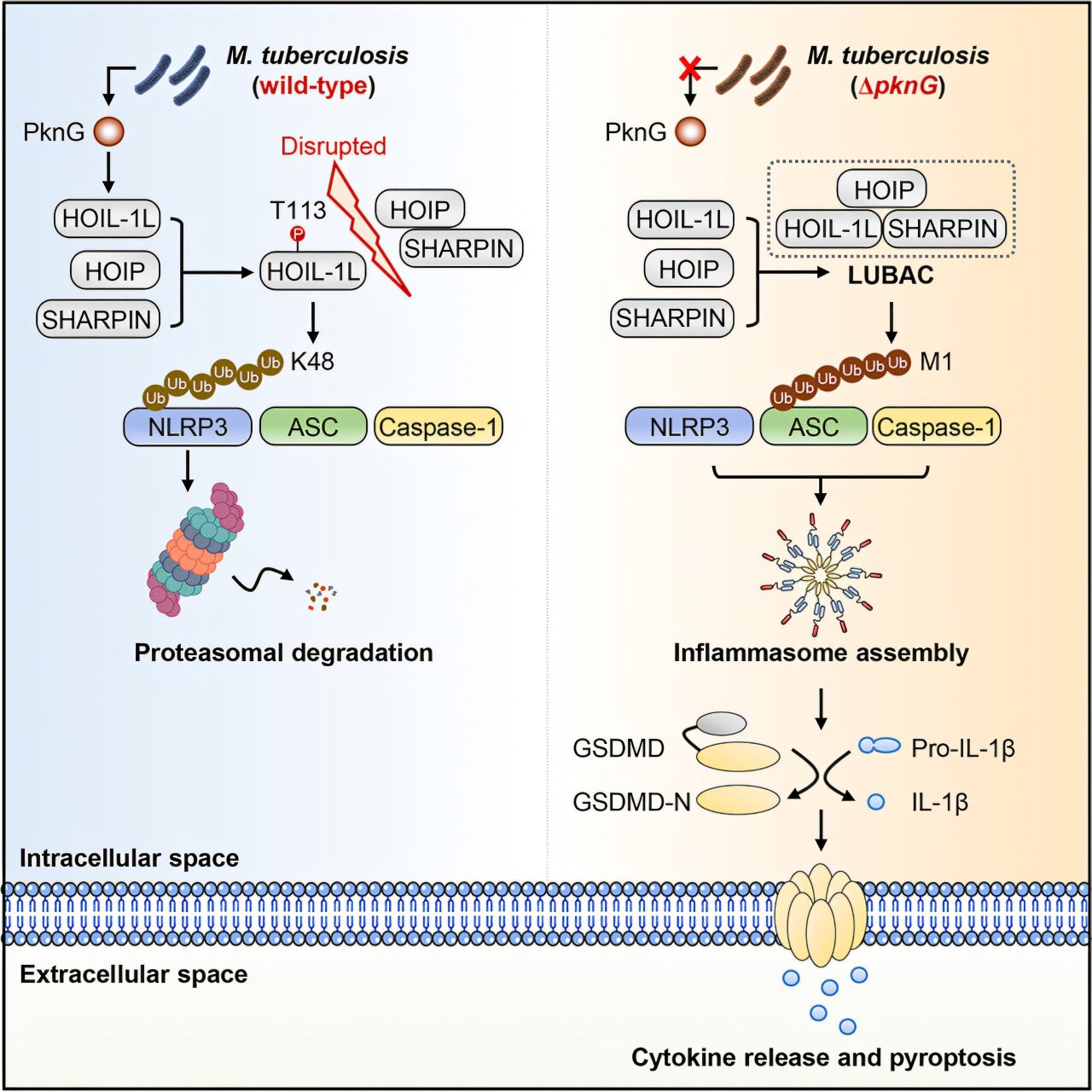
Dans cette étude, les chercheurs, dirigés par le professeur Liu Cuihua de l’Institut de microbiologie de l’Académie chinoise des sciences, ont constaté que PKNG, une protéine kinase sécrétée par le MTB, perturbe les réponses immunitaires médiées par le NLRP3 en interférant avec le complexe d’assemblage de la chaîne ubiquitine linéaire (Lubac).
Mécaniquement, PKNG phosphoryle la sous-unité HOIL-1L de Lubac, empêchant Hoil-1l de participer à la formation de Lubac. Cette perturbation altère l’ubiquitination linéaire dépendant du lubac de l’adaptateur inflammasome ASC, inhibant finalement l’assemblage inflammasome NLRP3.
De plus, la phosphorylation médiée par PKNG active simultanément l’activité intrinsèque de l’ubiquitine ligase de HOIL-1L, permettant à HOIL-1L de médier l’ubiquitination liée à K48 et une dégradation subséquente de NLRP3.
Pour résumer, grâce à ce mécanisme à double régulation qui réalise l’effet « une seule pierre-birds » comme mentionné ci-dessus, PKNG peut aider à promouvoir l’évasion du MTB de la surveillance immunitaire cytoplasmique médiée par NLRP3, facilitant ainsi davantage la survie intracellulaire et l’infection de l’agent pathogène.
Cette étude révèle que le MTB exploite la dynamique dépendante de la phosphorylation de la machinerie d’ubiquitine linéaire hôte par l’interaction PKNG / HOIL-1L. Cette interaction forme une cascade enzymatique inter-espèces qui entraîne une dégradation du capteur inflammasome, permettant au MTB de contrer la surveillance immunitaire dépendante du NLRP3.
Ces résultats fournissent également une stratégie potentielle pour le traitement anti-TB et l’optimisation du vaccin Bacille Calmette-Guérin (BCG) en ciblant l’interface PKNG / HOIL-1L.