Plus tôt cette année, des chercheurs de l’hôpital pour enfants de Philadelphie et de Penn ont créé un médicament unique en son genre adapté à une mutation génétique unique pour sauver un nourrisson nommé Baby KJ de la mort d’une maladie hépatique rare.
Les médecins de KJ Muldoon ont utilisé CRISPR, le raccourci à la mode pour un outil scientifique qui fonctionne comme une commande de recherche et de remplacement, pour localiser la faute d’orthographe génétique qui empêchait son corps de produire une enzyme clé qui décompose les protéines. Ils lui ont ensuite administré un médicament contenant des fragments de code génétique pour corriger la faute d’orthographe, améliorant ainsi considérablement ses chances de survie.
Le médicament ne sera jamais administré à un autre patient, mais les chercheurs pensent que l’approche pourrait être reproduite pour aider d’autres patients atteints de maladies rares, en personnalisant des médicaments sur mesure pour cibler différentes fautes d’orthographe génétiques.
Ils ont désormais un moyen de mettre leur théorie à l’épreuve. Le 12 novembre, la Food and Drug Administration des États-Unis a annoncé une nouvelle approche des essais cliniques pour tester des médicaments uniques en leur genre, comme celui que les médecins de CHOP et Penn ont créé pour KJ.
Cette approche ouvre la voie à l’approbation réglementaire – et à la couverture d’assurance – pour des traitements contre des maladies rares qui, dans le passé, auraient eu peu de chances d’atteindre le marché parce qu’ils profitent à si peu de personnes.
Le protocole de la FDA répond à un défi de longue date dans le développement de traitements pour les maladies rares : les scientifiques peinent à identifier suffisamment de patients pour créer une masse critique dans les essais, et les sociétés pharmaceutiques hésitent à investir des millions de dollars et des années dans le développement d’un médicament qui, en fin de compte, ne bénéficiera qu’à très peu de personnes.
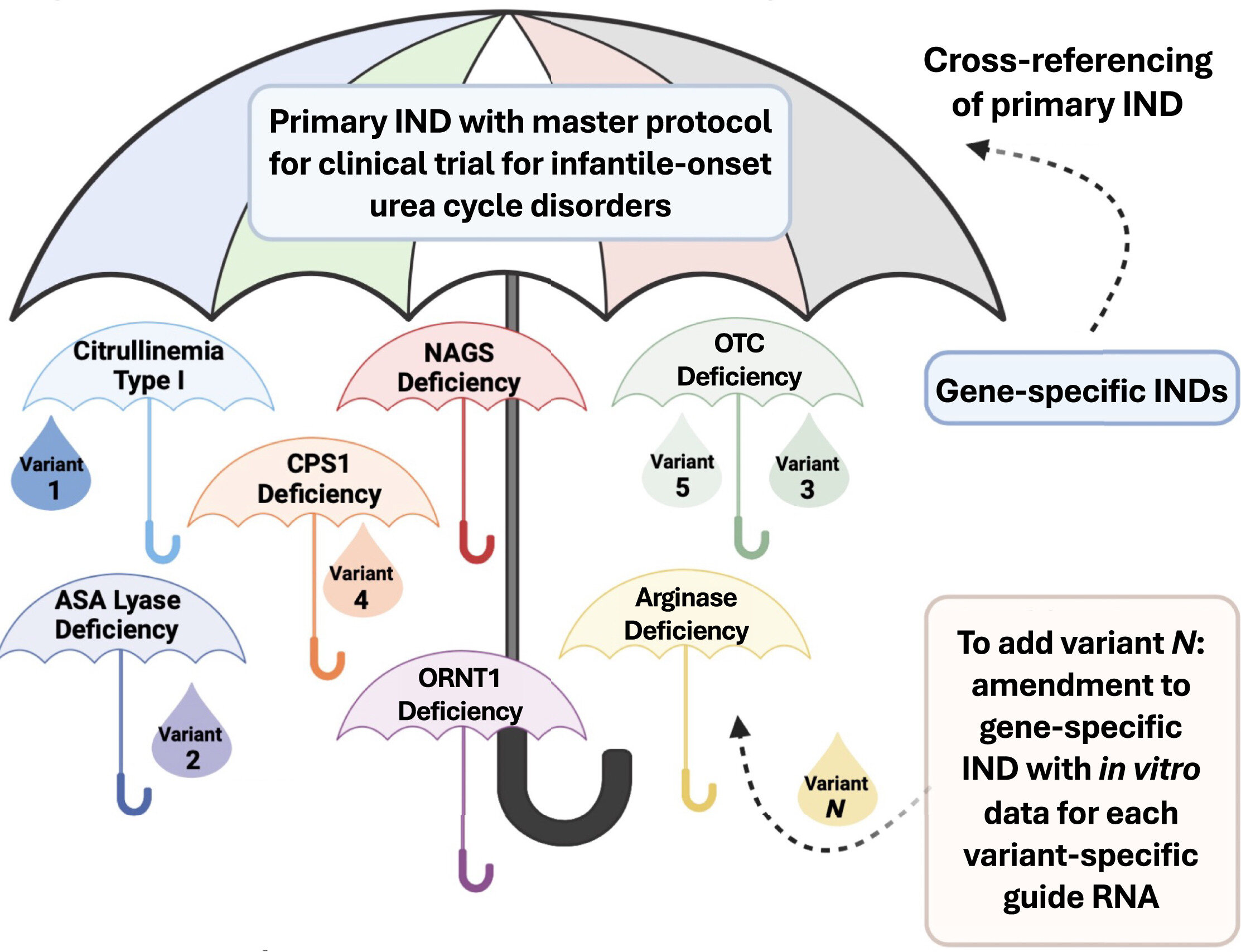
Désormais, le nouveau protocole de « mécanisme plausible » de la FDA permettra aux chercheurs de Philadelphie de tester le cadre CRISPR pour traiter les thérapies géniques personnalisées pour les troubles du cycle de l’urée liés à l’un des sept gènes. Le mécanisme restera le même, mais l’injection que chaque patient recevra sera personnalisée pour cibler sa mutation génétique unique.
L’équipe de Philadelphie, dirigée par Kiran Musunuru, cardiologue et expert en édition génétique à l’Université de Pennsylvanie, et Rebecca Ahrens-Nicklas, spécialiste des maladies métaboliques à l’hôpital pour enfants de Philadelphie, espère que leurs travaux serviront de modèle pour le développement de médicaments contre les maladies rares.
« En tant qu’universitaires, nous nous considérons comme le fer de lance, allant là où les entreprises hésitent à aller », a déclaré Musunuru.
Leur objectif, dit-il, est de montrer aux sociétés pharmaceutiques que le développement de médicaments contre les maladies rares est réalisable à plus grande échelle. Ils ont publié des détails sur leurs interactions avec la FDA dans le Journal américain de génétique humaine.
Bien que chaque maladie rare soit rare, des millions de personnes souffrent d’une maladie rare. Beaucoup ont des caractéristiques communes qui pourraient potentiellement être traitées grâce à un médicament personnalisable.
Utiliser CRISPR pour traiter les maladies rares
Le traitement de KJ était une nouvelle application de CRISPR, un outil d’édition génétique dont l’origine improbable implique des tests de contrôle qualité sur les bactéries utilisées dans la fabrication du yaourt.
Les scientifiques ont découvert que les bactéries conservent des enregistrements de l’ADN des virus qui les attaquent. Ces « clichés » microbiens peuvent être utilisés pour identifier une faute d’orthographe génétique dans l’ADN d’un patient.
Un type d’enzyme est ensuite utilisé pour « couper » la faute d’orthographe et la corriger ou l’éliminer.
Plus tôt cette année, les médecins de KJ ont annoncé qu’ils avaient utilisé cette technologie pour développer un médicament personnalisé en utilisant des informations sur sa mutation génétique spécifique.
Ils ont travaillé avec des partenaires externes de recherche et de fabrication pour produire rapidement le médicament et tester sa sécurité. Ils ont obtenu une autorisation accélérée de la FDA en vertu de règles conçues pour accélérer les traitements des maladies rares.
Cette approche a permis de sauver la vie de KJ, qui est rentré chez lui en juin après 307 jours d’hospitalisation et aura besoin d’un traitement continu.
Un médicament identique ne peut jamais être utilisé chez un autre patient. Et fabriquer des médicaments un par un pour les patients atteints de maladies rares n’est pas réalisable.
S’appuyer sur le traitement de KJ
Pour atteindre davantage de patients avec leur thérapie d’édition génétique, Musunuru et Ahrens-Nicklas devaient trouver un moyen de créer un médicament pouvant être produit à plus grande échelle.
De plus, ils devaient pouvoir demander l’approbation de la FDA, la référence en matière de sécurité des médicaments aux États-Unis, sans laquelle la plupart des compagnies d’assurance ne couvriraient pas les médicaments.
En règle générale, les développeurs de médicaments se concentrent sur un traitement spécifique pour une maladie spécifique, investissant des millions de dollars pendant une décennie maximum pour commercialiser le médicament.
Au lieu de cela, Musunuru et Ahrens-Nicklas ont travaillé avec la FDA pour créer un protocole d’essai qui leur permettrait de tester une plateforme médicamenteuse pouvant être personnalisée pour chaque patient.
« Le pouvoir du nombre est une chose réelle, pour pouvoir dire si un médicament est efficace », a déclaré Musunuru. « Si vous deviez tenter un procès pour chacun de ces sept cas, le coût serait prohibitif. »
Ils prévoient de conserver les mêmes éléments clés du traitement : CRISPR identifiera la faute d’orthographe génétique et les patients recevront un médicament contenant des morceaux d’ADN pour la corriger. Le gène exact ciblé dépendra du trouble spécifique de chaque patient.
Ils prévoient de tester le médicament sur des patients souffrant de troubles de l’urée, qui affectent la capacité du corps à décomposer les protéines et à excréter l’ammoniac, car ces conditions ont des « biomarqueurs » plus visibles, ou des indicateurs qui montrent quel est le problème et si la thérapie d’édition génique a aidé.
« Nous mesurons ce qui s’accumule et ce qui nous manque », a déclaré Ahrens-Nicklas.
Par exemple, KJ avait une mutation génétique qui empêchait son corps de créer une enzyme qui traitait les protéines. Les médecins pouvaient facilement vérifier que son corps manquait des enzymes nécessaires et que ses organes ne recevaient pas de protéines.
Après lui avoir administré le traitement sur mesure, ils ont pu constater que le nombre d’enzymes avait augmenté et que davantage de protéines étaient traitées.
Une nouvelle voie FDA pour le traitement des maladies rares
Dans un Journal de médecine de la Nouvelle-Angleterre Dans un article décrivant leur plan, le commissaire de la FDA, Marty Makary, et Vinay Prasad, directeur médical et scientifique de l’agence, ont cité la thérapie génique pour un seul patient de KJ comme exemple de la manière dont ils espèrent que le nouveau protocole contribuera à atteindre davantage de patients.
Le traitement de KJ a été initialement approuvé par la FDA dans le cadre d’un processus d’examen accéléré d’une semaine conçu pour être utilisé pour un seul patient, généralement un patient gravement atteint d’une maladie ultra rare.
Prasad et Makary ont écrit que « les réglementations actuelles sont onéreuses et inutilement exigeantes, offrent une protection peu claire aux patients et étouffent l’innovation ».
Le cas de KJ « met en évidence le potentiel » de développement de thérapies pour un seul patient en un médicament qui pourrait être modifié pour traiter d’autres maladies rares similaires, ont-ils écrit.
« Près de 30 ans après le séquençage du génome humain, les thérapies sur mesure sont proches de la réalité », écrivent-ils.