La tuberculose (TB) est l’une des maladies infectieuses les plus courantes au monde. Bien que l’infection par la bactérie Mycobacterium tuberculosis affecte principalement les poumons, jusqu’à 25 % de toutes les personnes infectées en seront également atteintes dans d’autres parties de leur corps, comme les ganglions lymphatiques, les os ou le cerveau. Dans le monde entier, environ 10 millions de personnes contractent la tuberculose chaque année, dont 1,25 million mourront des suites de leur infection.
Cependant, jusqu’à présent, la réponse immunitaire à la tuberculose, et en particulier à l’EPTB, n’a pas été suffisamment comprise. Dans certaines régions du monde, jusqu’à 30 % des personnes atteintes de tuberculose souffrent d’EPTB, qui peut affecter tous les organes en dehors des poumons. Cela rend le diagnostic et le traitement beaucoup plus difficiles, car il n’existe pas de biomarqueurs facilement accessibles.
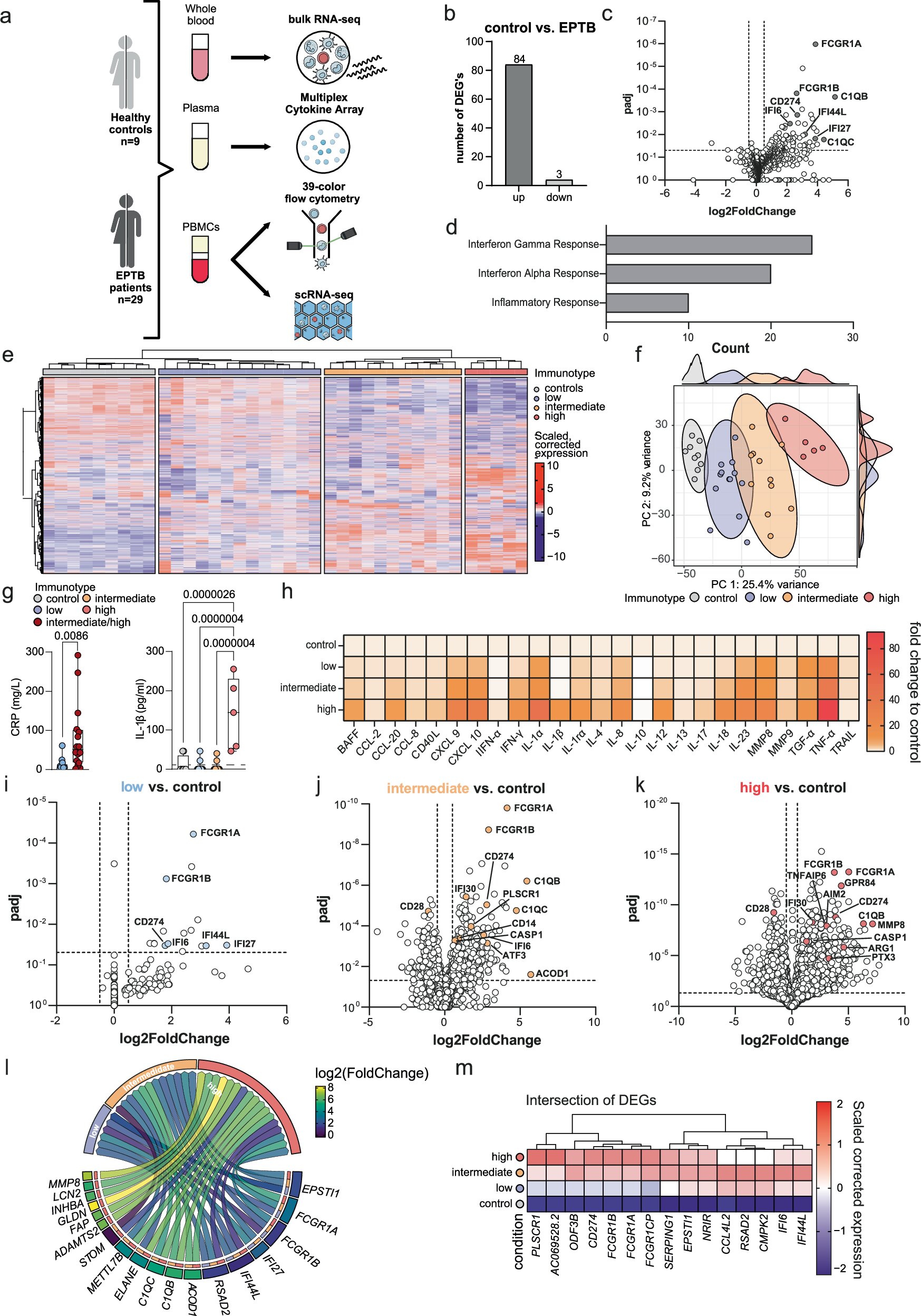
Pour mieux comprendre les processus immunologiques en jeu, les chercheurs ont étudié le sang des patients atteints d’EPTB en utilisant des approches multi-omiques de pointe telles que le séquençage de l’ARN unicellulaire des cellules sanguines. Leur analyse des données du transcriptome a révélé des réseaux de signalisation complexes entre les parties concernées du système immunitaire qui jouent un rôle important dans la lutte contre les agents pathogènes et le contrôle de l’inflammation.
L’ouvrage est publié dans la revue Communications naturelles.
L’immunotypage fournit de nouvelles informations sur les mécanismes de la maladie
Le Dr Sebastian Theobald, premier auteur de l’étude et associé de recherche à l’hôpital universitaire de Cologne, déclare : « Les données nous ont permis pour la première fois d’attribuer aux patients EPTB l’un des trois immunotypes distincts qui reflètent différentes progressions de la maladie. »
Le professeur Jan Rybniker, chef du domaine d’intervention pour les maladies infectieuses cliniques à l’hôpital universitaire de Cologne et coordinateur adjoint du domaine de recherche sur la tuberculose au DZIF, ajoute : « Cette dynamique facilite de nouvelles connaissances sur le mécanisme de la tuberculose et nous permettra, espérons-le, d’offrir aux patients un traitement personnalisé et plus efficace à l’avenir.
Le co-auteur Kilian Dahm, bioinformaticien à l’hôpital universitaire de Bonn et au DZNE, a contribué aux recherches de l’étude au cours de son doctorat à l’université de Bonn : « En particulier, l’interaction entre les voies de signalisation de l’interféron et de l’interleukine-1 et l’activation des lymphocytes T et des cellules tueuses naturelles ont joué un rôle clé dans l’identification des immunotypes. »
Les signatures moléculaires dans le sang permettent de nouvelles méthodes de diagnostic
Les chercheurs ont réussi à développer des biomarqueurs basés sur l’expression génique capables de diagnostiquer de manière fiable la tuberculose extrapulmonaire et pulmonaire. Dans l’état actuel des choses, les patients doivent subir une biopsie tissulaire pour recevoir un diagnostic d’EPTB. À l’avenir, cependant, l’identification de signatures basées sur des marqueurs immunologiques et des modèles d’expression génique dans le sang pourrait servir de biomarqueurs facilement accessibles pour diagnostiquer l’EPTB et avoir ainsi un impact majeur sur les soins aux patients.
Le Dr Thomas Ulas est bioinformaticien au DZNE et à l’Institut LIMES de l’Université de Bonn et membre du pôle d’excellence ImmunoSensation2 de l’université. Il déclare : « Nos résultats contribueront à améliorer considérablement le diagnostic et le traitement de la tuberculose et ouvriront la voie à des thérapies ciblées et adaptées. »
Privatdozent Dr. Isabelle Suárez, médecin-chef de la Clinique I de médecine interne de l’hôpital universitaire de Cologne, ajoute : « La caractérisation clinique des patients était cruciale pour catégoriser correctement les résultats moléculaires et combler le fossé avec la pratique clinique.
Les découvertes sur le diagnostic des signatures moléculaires dans le sang des patients EPTB qui ont été glanées à partir des investigations menées jusqu’à présent sont actuellement soumises à une validation plus approfondie dans le cadre d’une cohorte clinique à grande échelle connue sous le nom d’étude mEx-TB. Dirigé par Rybniker et Suárez, il est basé dans plusieurs centres DZIF en Allemagne.