Aux États-Unis, environ 12 millions d’adultes sont touchés par le SSPT, ce qui a un impact entre 4% et 8% de la population adulte, et jusqu’à 30% du personnel militaire et des anciens combattants. De manière frappante, 63% des anciens combattants atteints de troubles de stress post-traumatique souffrent également d’un trouble de la consommation d’alcool (AUD) et / ou d’une douleur chronique. Ces conditions se chevauchent fréquemment, avec des individus qui souffrent de douleurs AUD ou chroniques qui éprouvent également du SSPT.
Lorsque ces troubles co-occupent, ils ont tendance à aggraver les uns les autres, ce qui rend un traitement efficace beaucoup plus difficile. Actuellement, aucun médicament approuvé ne traite efficacement le SSPT et l’AUD ensemble, et de nombreux médicaments disponibles sont livrés avec des effets secondaires graves ou des résultats limités.
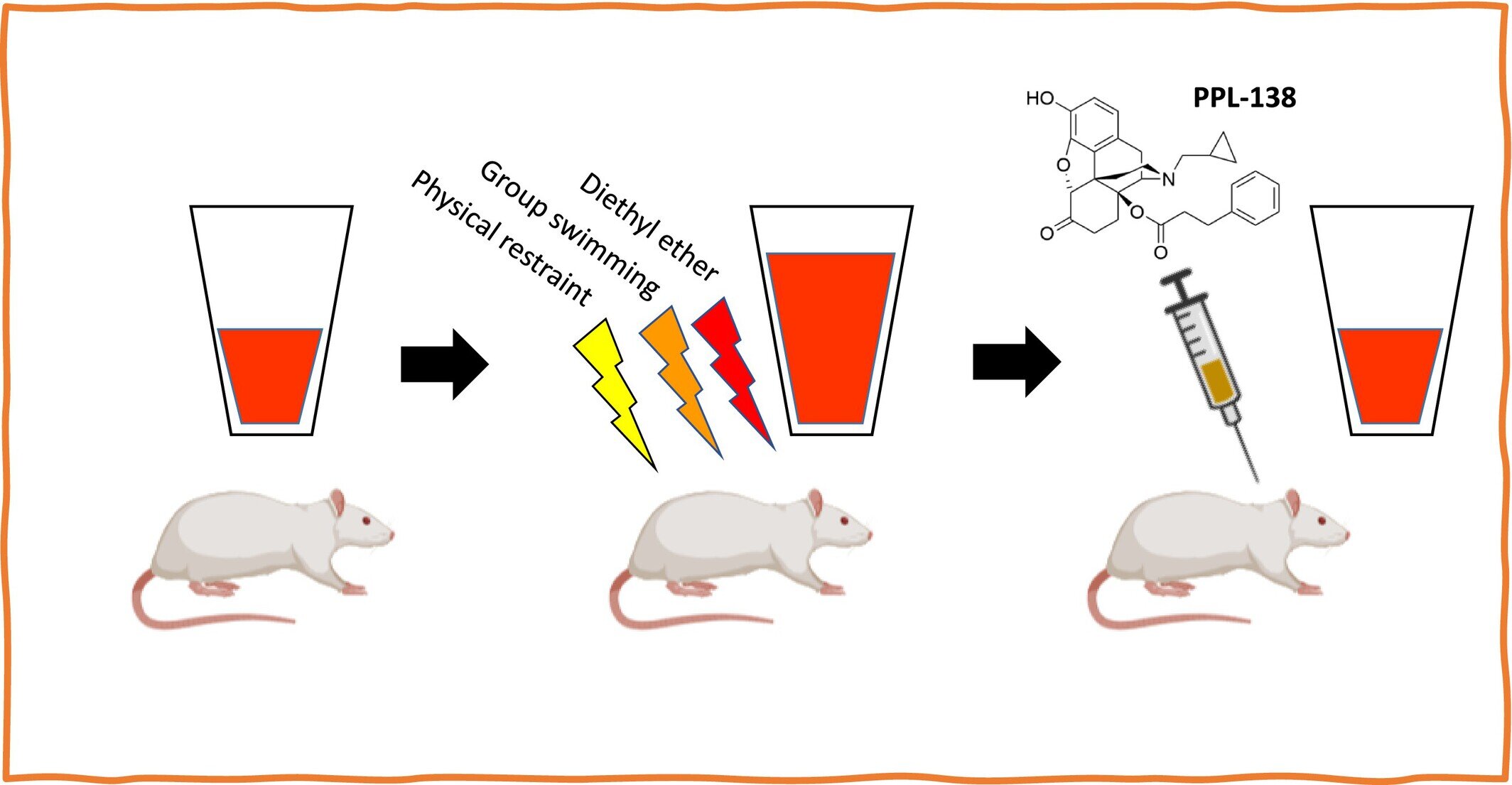
Des chercheurs du Charles E. Schmidt College of Medicine de la Florida Atlantic University, en collaboration avec le College of Pharmacy de l’Université de l’Oklahoma, ont mené deux études complémentaires chez le rat pour explorer comment un nouveau médicament, PPL-138, pourrait aider à traiter le SSPT et ses compagnons communs – l’anxiété, la douleur chronique et l’AUD. Type d’agoniste partiel opioïde, PPL-138 fonctionne en ciblant des récepteurs opioïdes spécifiques dans le cerveau.
La propriété intellectuelle liée à PPL-138 appartient à Phoenix Pharmalabs, Inc. La société est en train de faire progresser PPL-138 à travers des essais cliniques.
La première étude, réalisée à l’Université d’Oklahoma, a examiné si le traitement à long terme avec PPL-138 pourrait réduire les symptômes liés au SSPT dans le stress traumatique chronique. La deuxième étude, menée au FAU, s’est concentrée sur la relation entre les traumatismes, l’anxiété et la consommation d’alcool, et les chercheurs ont divisé les rats en différents groupes.
Résultats, publiés dans le Journal britannique de pharmacologiefournissez des preuves prometteuses que le PPL-138 pourrait devenir un traitement précieux pour le SSPT et l’abus d’alcool, en particulier lorsque les symptômes sont enracinés dans l’anxiété. En ciblant un système cérébral impliqué à la fois dans le stress et la toxicomanie, les chercheurs pensent que le PPL-138 pourrait un jour offrir une percée bien nécessaire pour ceux qui luttent avec ces conditions qui changent la vie.
Les résultats montrent que le PPL-138 a considérablement réduit le comportement de type anxiété, les réponses à la douleur et la consommation d’alcool, mais seulement chez les rats qui ont développé des symptômes de type SSPT. Chez les rats mâles et femelles, le médicament a réduit sélectivement la consommation d’alcool dans ceux qui ont également montré des signes d’anxiété liée au traumatisme, sans affecter ceux qui étaient résilients ou non stressés.
« Nos résultats montrent que le PPL-138 réduit non seulement l’anxiété et la douleur liées aux traumatismes, mais aussi sélectivement la consommation d’alcool chez le rat le plus vulnérable à la consommation d’alcool induite par le stress », a déclaré Andrea Cippitelli, Ph.D., auteur principal et professeur adjoint au Département des sciences biomédicales du Schmidt College of Medicine et membre du Fau Stiles-Nicholson Brain Institute.
« Ce type de traitement ciblé pourrait transformer la façon dont nous gérons le SSPT et ses comorbidités, en particulier pour le grand nombre de patients qui tombent actuellement à travers les mailles du filet des thérapies existantes. »
Les résultats de l’étude soulignent également la nécessité de considérer les différences sexuelles dans les causes et le traitement de ces conditions de chevauchement. Parmi les rats femelles, le PPL-138 a réduit l’apport d’alcool chez ceux qui présentent de l’anxiété, même si leur consommation d’alcool ne s’était pas dégénérée. Cela indique que l’anxiété seule peut être un facteur primaire à l’origine de la consommation d’alcool chez les femmes.
« Les rats mâles anxieux étaient deux fois plus susceptibles que les femmes pour augmenter leur consommation d’alcool après un traumatisme, tandis que presque toutes les rats femelles avec plus de consommation d’alcool ont également montré des signes clairs d’anxiété », a déclaré Cippitelli. « Cela reflète des schémas bien documentés chez l’homme, où les femmes sont plus sujettes aux troubles liés à l’anxiété comme le SSPT et consomment souvent de l’alcool pour faire face à la détresse émotionnelle, tandis que les hommes s’engagent généralement dans une consommation d’alcool plus lourde et plus généralisée. »
Surtout, les effets de PPL-138 n’étaient pas dus à la sédation ou à l’activité réduite. Le composé n’a pas modifié le mouvement ou la consommation d’alcool chez les rats avec des comportements liés à l’anxiété ou un stress traumatique. En fait, les niveaux de mouvement sont restés inchangés chez les rats mâles et ont légèrement augmenté chez les femmes – soutenant l’idée que le médicament agit spécifiquement sur les comportements liés au stress et à l’anxiété, plutôt que de provoquer une suppression générale ou une sédation.
« Cette recherche représente une étape indispensable pour aider les civils et les anciens combattants vivant avec les blessures invisibles du traumatisme », a déclaré Cippitelli. « Dans nos études précliniques, PPL-138 montre un fort potentiel en tant que thérapie unique pour les symptômes de chevauchement du SSPT, de la douleur chronique et de l’abus d’alcool – offrant une alternative potentiellement plus sûre et plus efficace aux approches multi-médicaments actuelles. »
Les co-auteurs de l’étude sont Yong Zhang, Ph.D., Université de l’Oklahoma College of Pharmacy; Kyle Kealoha, un doctorat. étudiant du Département des sciences biomédicales du FAU; Ali Idriss, ancien technicien de laboratoire de recherche, FAU Département des sciences biomédicales; Panini S. Patankar, MD, Université de l’Oklahoma College of Pharmacy; Benjamin Carper, RTI International, Research Triangle Park; Lawrence Toll, Ph.D., professeur de sciences biomédicales, Schmidt College of Medicine et membre du Fau Stiles-Nicholson Brain Institute; et Kelly M. Stanfer, Ph.D., Université de l’Oklahoma College of Pharmacy.