Une équipe multidisciplinaire internationale a démontré pour la première fois que l’activation des gènes basée sur CRISPR (CRISPRA) peut être utilisée pour traiter les maladies cardiaques génétiques in vivo. L’étude, publiée dans le European Heart Journal et présenté au Congrès de la Société européenne de cardiologie à Madrid, ouvre la voie à de nouvelles thérapies ciblées pour les patients atteints de troubles cardiaques génétiques. Cette approche pourrait être particulièrement utile pour les patients présentant des conditions causées par des mutations dans les gènes trop importants pour être ciblés avec une thérapie génique conventionnelle.
L’équipe était dirigée par des scientifiques du Centro Nacional de Investigaciones Cardiovasculares (CNIC), avec la participation des scientifiques de l’hôpital Universitario Puerta de Hierro et de l’Université de Californie San Diego.
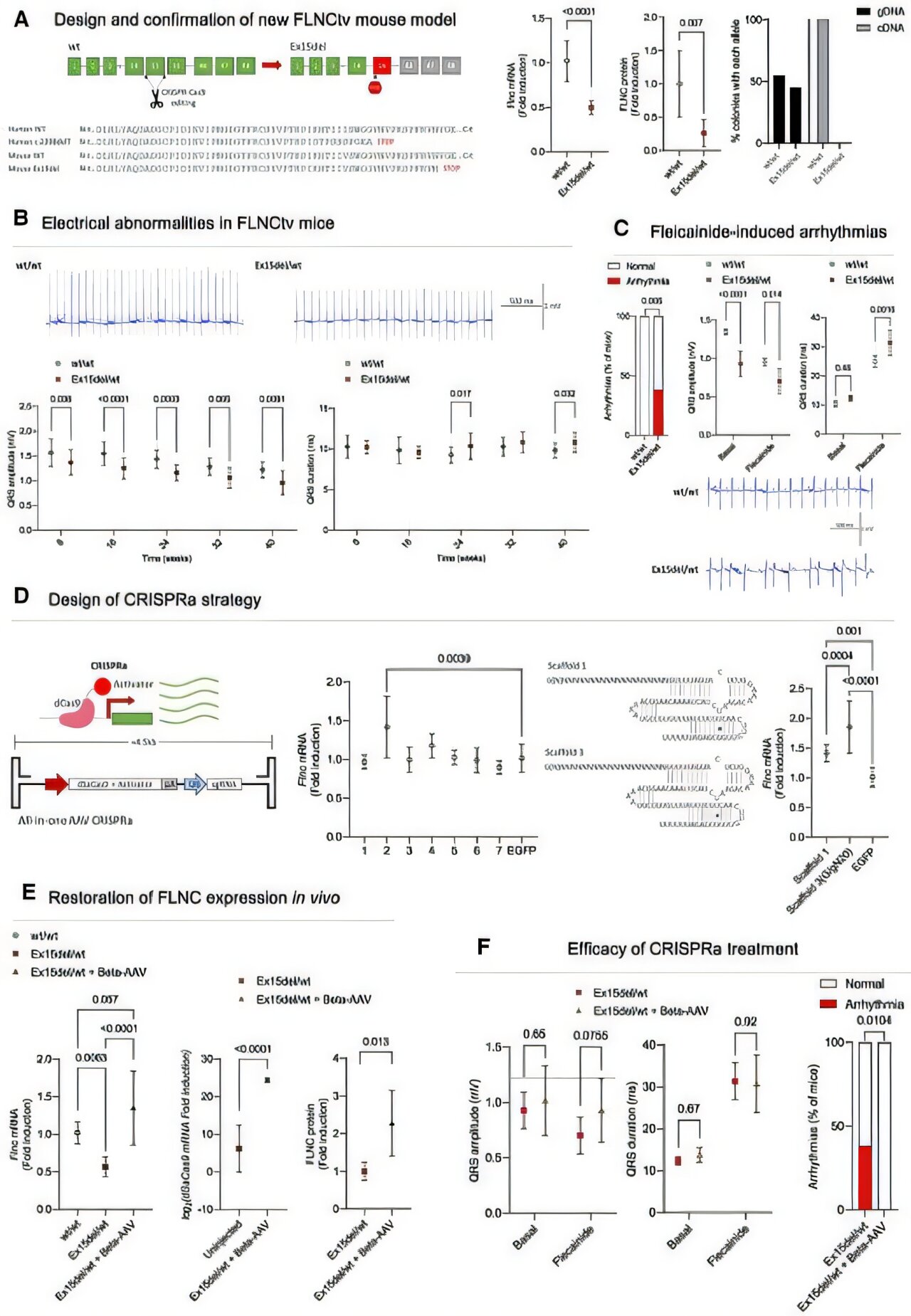
L’équipe a fait cette découverte dans un nouveau modèle animal qu’ils ont développé qui porte une mutation tronquée dans le gène Filamin C (FLNC). Les variantes tronquées dans le FLNC (FLNCTV) réduisent la quantité de protéine de filamine C produite et sont une cause fréquente de cardiomyopathie dilatée génétique et de cardiomyopathie ventriculaire non dilisée gauche. Les deux maladies prédisposent les patients à des arythmies sévères et augmentent le risque de mort cardiaque soudaine. Il n’y a actuellement aucune thérapie spécifique disponible pour ce type de mutation, et les options cliniques sont limitées aux traitements généraux de l’insuffisance cardiaque et aux dispositifs de défibrillateur implantables.
Les chercheurs ont développé un modèle de souris portant une mutation de FLNC tronquée qui reproduit les anomalies électriques observées chez les patients, y compris une vulnérabilité accrue aux arythmies induites par les médicaments.
Pour restaurer la fonction des gènes, l’équipe a conçu un système de thérapie génique basé sur CRISPRA emballé dans un virus adéno-associé cardiotrope (AAVMYO). « Ce système ne coupe pas l’ADN », explique le premier auteur de l’étude, le Dr Rodrigo Cañas Álvaro, « mais utilise plutôt une protéine CRISPR inactive inactive à un activateur transcriptionnel pour allumer le promoteur FLNC, augmentant ainsi la production de filamines dans le cœur. »
Après l’administration du vecteur aux souris mutantes adultes, les chercheurs ont observé une normalisation de l’ARN de FLNC et l’expression des protéines aux niveaux trouvés chez les animaux en bonne santé. Les enregistrements d’électrocardiogramme ont montré la récupération de l’amplitude QRS et, surtout, la disparition complète des arythmies induites par le flécaïnide.
« Cette étude démontre pour la première fois que l’activation du gène CRISPRA peut inverser les manifestations d’une cardiomyopathie héréditaire dans un modèle animal », explique le Dr Lara-Pezzi, un chercheur CNIC et CiberCV et l’auteur principal de l’étude. « Nos résultats suggèrent que même après que la maladie s’est développée, il est possible de restaurer la fonction électrique du cœur à travers une approche ciblée. »
Le collaborateur de l’étude, le Dr Pablo Garcia-Pavía, la tête de l’unité des maladies cardiaques héréditaires de l’hôpital Universitario Puerta de Hierro, CNIC et CiberCV Investigator – vole la signification des résultats. « Cette recherche établit la base du développement des thérapies CRISPRA-AAV non seulement pour les mutations FLNC mais aussi pour d’autres troubles cardiaques causés par une production insuffisante de protéines essentielles qui ne peuvent pas être ciblées par la thérapie génique conventionnelle. »