Par Rhys Thomas White, Juliet Elvy, Kristin Dyet, Maria Hepi, Nigel French, Sarah Bakker, The Conversation
Après une césarienne de routine dans un hôpital d’Auckland, une mère a développé une douleur intense et ce qui semblait être une fatigue postnatale. Il s’est avéré être une infection par Staphylococcus aureus résistant à la méthicilline (SARM), un « superbactif » se propageant à travers la Nouvelle-Zélande et au-delà.
Son histoire n’est pas unique. À Dunedin, une autre mère a reçu un diagnostic de SARM et de saignement interne post-partum.
Ce sont des histoires personnelles, mais ce sont également des signaux d’alerte précoce d’un défi de sécurité pour la santé plus large.
La méthicilline est un antibiotique de la famille de la pénicilline, et le SARM y résiste (et souvent à d’autres types d’antibiotiques). Cela rend les infections plus difficiles à traiter.
Autrefois considérées comme principalement un problème d’hôpital, les infections résistantes à la méthicilline sont désormais courantes dans la communauté.
Une souche du SARM qui a émergé en Nouvelle-Zélande (nommée AK3) est désormais la tension dominante dans nos communautés. Les habitudes de dispense des antibiotiques du pays peuvent l’avoir aidé à émerger et à se propager.
Une tension d’origine néo-zélandaise avec une portée mondiale
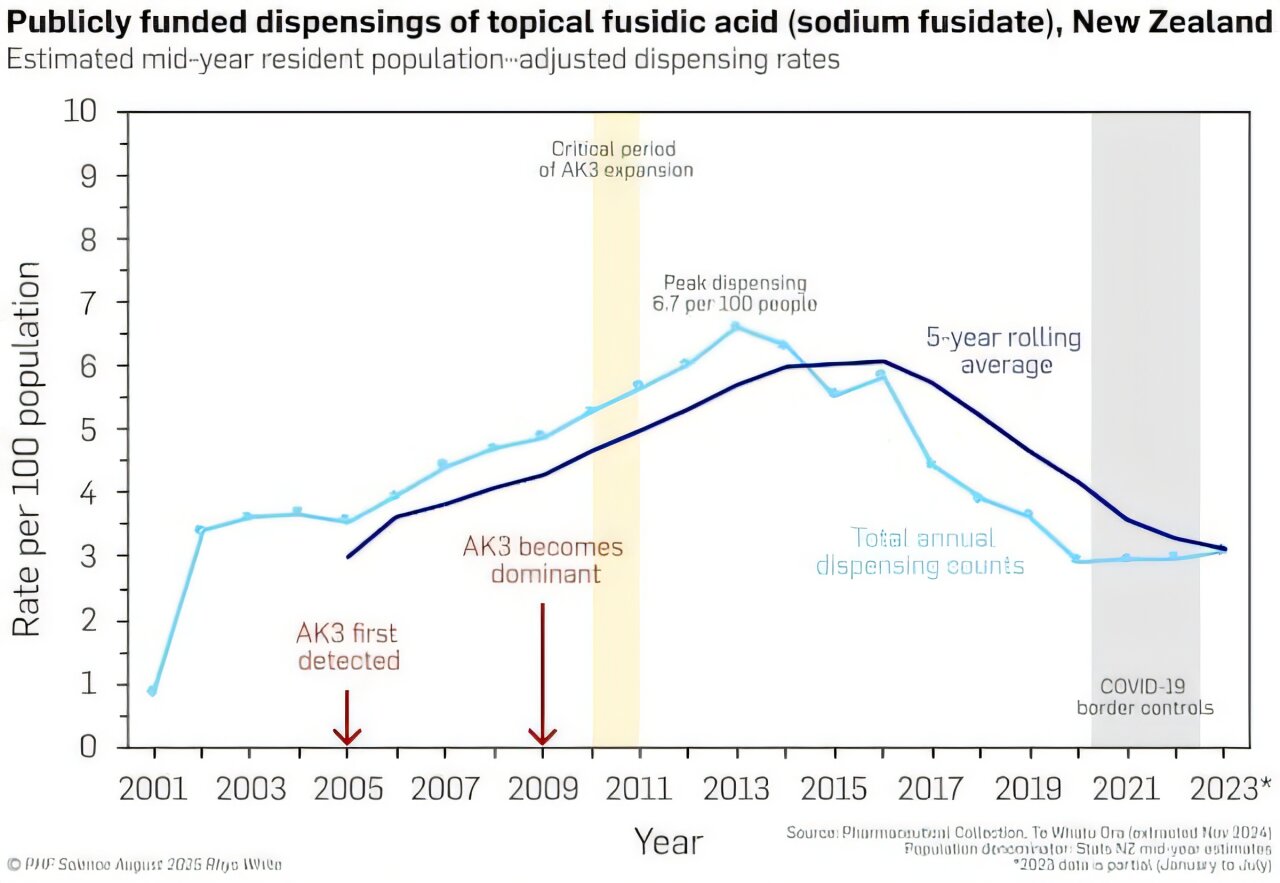
L’AK3 a été détectée pour la première fois en 2005. Aujourd’hui, c’est la principale cause d’infections du SARM en Nouvelle-Zélande et, comme le montre notre nouvelle étude, a également été détectée dans le Pacifique Sud et en Europe.
En utilisant le séquençage du génome entier, nous avons tracé le voyage d’Ak3 d’un ancêtre sensible à la médicament à un clone très résistant. En cours de route, Ak3 a acquis des gènes de résistance clés, y compris ceux conférant une résistance à la méthicilline et à l’acide fusidique, un antibiotique topique autrefois prescrit à des taux historiquement élevés en Nouvelle-Zélande.
La distribution de l’acide fusidique topique a diminué depuis 2016. Mais une fois que la résistance devient courante, il peut être difficile de réduire ou de revenir sous une forme sensible. C’est pourquoi il est si important de préserver l’efficacité des antibiotiques en les utilisant soigneusement et uniquement en cas de besoin (une pratique connue sous le nom de l’intendance antimicrobienne), et de surveiller les tendances de la résistance en utilisant la surveillance génomique.
Comment une prescription commune a aidé une superbacte à prospérer
En Nouvelle-Zélande, l’acide fusidique était autrefois largement prescrit dans la communauté pour traiter les infections cutanées, souvent sans diagnostic confirmé. Cette utilisation généralisée a créé des conditions idéales pour la résistance à l’acide fusidique pour se développer.
L’émergence de Ak3 montre comment les antibiotiques, lorsqu’ils sont surutilisés à l’échelle nationale, peuvent conduire l’évolution d’une résistance mondiale significative. Notre étude génomique a amélioré notre compréhension de l’évolution de l’AK3 et est devenue dominante en Nouvelle-Zélande.
Nos analyses et données de santé publique montrent que AK3 n’affecte pas tous les groupes également. Par rapport aux personnes d’ethnicité européenne, les Maoris sont trois fois plus susceptibles et les peuples du Pacifique presque cinq fois plus probablement, pour souffrir d’infections cutanées causées par S. aureus.
Les facteurs socio-économiques amplifient le risque: ceux des zones les plus défavorisées sont près de quatre fois plus susceptibles d’être hospitalisés pour les infections cutanées.
Le fardeau des infections cutanées et la surutilisation de l’acide fusidique ont créé les conditions pour Ak3 pour émerger, s’adapter et se propager. Pour les personnes atteintes d’Ak3 et d’autres superpousses résistantes, il est essentiel de préserver l’efficacité des antibiotiques. L’acide fusidique a toujours un rôle dans le traitement, mais l’objectif est de trouver le bon équilibre entre le sous-prescription et la surescription.
S’attaquer à cela nécessite un accès amélioré à des soins et un traitement appropriés en temps opportun dans les communautés les plus touchées. C’est un rappel que même les technologies les plus avancées ne peuvent pas, à elles seules, surmonter les barrières structurelles. Si nous sommes sérieux au sujet de la menace des pose de résistance antimicrobienne, nous devons affronter ces inégalités frontal.
Quoi de suivi?
Récemment, nous avons détecté Ak3 dans un échantillon de lait cru prélevé directement dans une vache avec mammite pendant les tests vétérinaires – bien avant tout traitement, et non à partir du lait destiné aux personnes à boire. Les gènes de résistance peuvent franchir les frontières humaines, animales et environnementales, ce qui exige une approche «une santé», intégrant la surveillance avec une politique et une action coordonnées dans tous les domaines.
La surveillance est la collecte continue et systématique de données pour éclairer l’action de santé publique, en s’appuyant généralement à partir de sources multiples, notamment des résultats de laboratoire, des informations épidémiologiques et une analyse génomique.
La montée de l’AK3 souligne la nécessité d’une stratégie de résistance antimicrobienne proactive et intégrée à travers la science, la politique, la santé vétérinaire et publique. La génomique est une priorité stratégique clé, soutenant une approche fondée sur des preuves des maladies actuelles et émergentes.
Le cas d’AK3 met ces priorités à se concentrer et montre pourquoi une action coordonnée est essentielle pour rester en avance sur les menaces émergentes.
Pour protéger la sécurité et l’économie pour la santé de la Nouvelle-Zélande, nous devons soutenir une utilisation antimicrobienne appropriée. L’antibiotique droit doit être utilisé au bon moment et à la bonne dose, guidé par des données locales sur la résistance microbienne et soutenue par des diagnostics accessibles.
Nous devons également étendre la surveillance de la résistance aux antimicrobiens et renforcer la surveillance de la santé humaine, animale et environnementale, avec l’analyse génomique comme composant central afin que les menaces puissent être détectées et la transmission perturbée plus tôt.
Les histoires de deux mères dont les infections au SARM complexes compliquaient l’accouchement sont plus que des études de cas. Ce sont des appels à l’action et AK3 est notre test. Il nous met au défi de passer du traitement réactif à la prévention proactive.
La Nouvelle-Zélande a les outils, les talents, la technologie et les réseaux à diriger dans la surveillance et la réponse des antimicrobiens. Mais nous devons agir de manière décisive. Pas seulement pour contenir AK3, mais pour empêcher le prochain superbogue d’émerger.
Traitons les antibiotiques comme l’infrastructure critique qu’ils sont, reconnaissant que le pipeline pour de nouveaux antibiotiques est très étroit. Nous devons nous assurer que les antibiotiques fonctionneront toujours lorsque nous en aurons le plus besoin.