Traitement avec l’interféron ou avec de l’acétate de glatirame? Cette question se pose pour de nombreux patients qui reçoivent un diagnostic de sclérose en plaques (SEP) pour la première fois. Jusqu’à présent, le choix entre les deux pourrait être pratiquement fait au hasard: les deux préparations sont considérées comme des thérapies de base établies, les deux ont des effets secondaires relativement faibles et les deux sont relativement bien tolérés. Et, comme pour toutes les thérapies immunomodulatrices, les deux n’aident pas toutes les personnes aussi bien. Cependant, grâce à une étude dirigée par l’Université de Münster, il y a maintenant un critère clair pour le choix du médicament.
Le groupe de recherche international a identifié un biomarqueur génétique qui prédit si les patients atteints de SEP réagiront particulièrement bien au traitement par l’acétate de glatiramerie (GA). Les personnes atteintes de type tissulaire HLA-A * 03: 01 bénéficient beaucoup plus de GA que de l’interféron bêta (IFN-β). Les résultats de l’analyse multicentrique de plus de 3 000 patients atteints de SEP ont maintenant été publiés dans la revue ebiomedicine.
« Notre étude montre pour la première fois qu’un marqueur génétique est lié au succès du traitement d’un médicament MS », explique le chef de l’étude, le professeur Nicholas Schwab de l’Université de Münster. « Cela nous permet de prédire avant de commencer la thérapie si l’acétate de glatiamère ou l’interféron est probablement le meilleur choix. »
Chez environ 1 patients atteints de MS sur 3, la décision remonte à GA et, dans les deux autres cas, l’interféron bêta est probablement plus efficace. « Il s’agit d’une avancée significative pour le traitement personnalisé de la SEP », explique le professeur Heinz Wiendl, porte-parole du Network de compétence allemand sur la sclérose en plaques, qui a conçu l’étude.
Avantage clinique confirmé dans cinq cohortes indépendantes
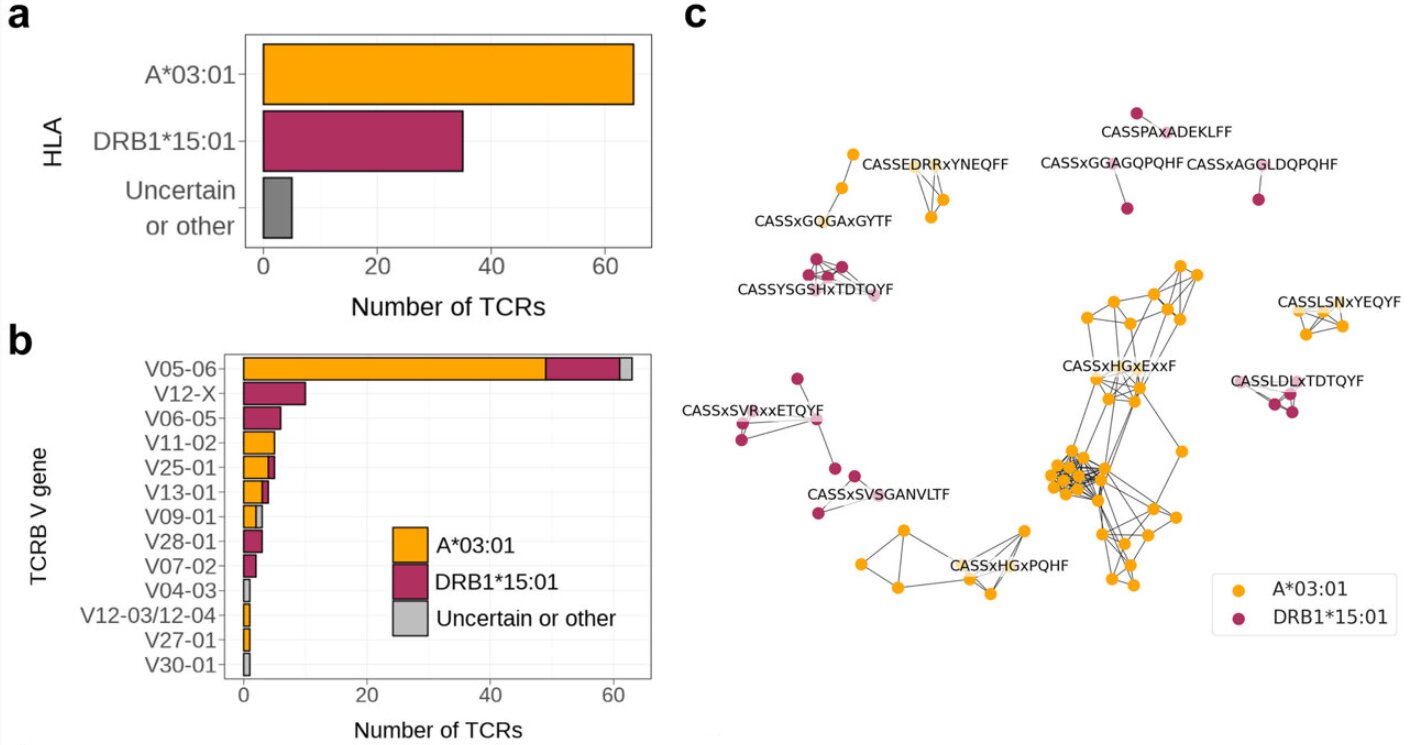
L’AG conduit à des réponses spécifiques des cellules T chez les patients, que l’équipe a examiné de plus près. Les chercheurs ont analysé les séquences des récepteurs des cellules T (TCR) dans le sang de 3 021 patients atteints de SEP, dont les échantillons ont été fournis à partir de plusieurs cohortes internationales distinctes. Des clones de cellules T ont été identifiés qui ont été trouvés après le traitement par GA uniquement chez les patients qui transportaient également des molécules HLA spécifiques, à savoir HLA-A * 03: 01 ou HLA-DRB1 * 15: 01.
Si l’une de ces deux molécules HLA est présente, le système immunitaire réagit ainsi à la thérapie GA. Cependant, pratiquement, les patients ne bénéficient que dans l’un des deux cas: seuls les patients atteints de SEP avec la variante du gène HLA-A * 03: 01 ont un bénéfice de traitement clinique éprouvé, c’est-à-dire qu’ils s’améliorent en raison de la thérapie par GA.
Pour s’assurer que les résultats sont également pertinents dans l’application clinique, l’équipe a examiné cinq grandes cohortes et des populations d’étude des États-Unis, de la France et de l’Allemagne, y compris la cohorte Nationms de la sclérose en plaques du réseau de compétences allemands. Dans toutes les analyses, les porteurs de la variante du gène HLA-A * 03: 01 ont montré significativement moins de symptômes de la maladie sous traitement GA par rapport au traitement IFN-β. Statistiquement, cela affecte environ 30 à 35% des patients atteints de SEP européens car ils portent l’allèle HLA-A * 03: 01.
Décision de thérapie personnalisée possible grâce à des tests génétiques simples
Ce qui est spécial dans cette découverte, c’est que le nouveau résultat de recherche peut déjà être appliqué dans la consultation thérapeutique à court terme – parce qu’un test HLA, qui est déjà établi pour les transplantations ou la sécurité des médicaments, par exemple, détecte la variante de gènes pertinente.
Cependant, les connaissances acquises par l’étude atteignent encore plus. Il fournit non seulement un biomarqueur cliniquement pertinent, mais aussi de nouveaux indices sur le mécanisme d’action de GA – les réponses publiques observées des cellules T suggèrent que GA n’a pas besoin que tous ses composants protéiques fonctionnent. Au lieu de cela, seuls quelques fragments du mélange GA jouent un rôle dominant, peut-être même un seul. À l’avenir, cela pourrait conduire à la poursuite du développement ciblé du médicament.