Les chercheurs en virologie de la clinique de Cleveland ont découvert qu’une modification spécifique des protéines de la protéine immunitaire MDA5 est la clé de la façon dont les corps humains détectent et répondent aux virus et à la réplication virale.
Le Actes de l’Académie nationale des sciences La publication explique comment deux modifications des protéines activent le MDA5, une protéine immunitaire essentielle, pour détecter les envahisseurs, limiter la réplication virale et lutter contre les infections. Ce processus est essentiel pour prévenir les résultats comme l’inflammation cardiaque induite par le virus.
Cette publication la plus récente s’appuie sur un ensemble d’œuvres du laboratoire de Michaela Gack, Ph.D., directeur scientifique du Cleveland Clinic’s Florida Research & Innovation Center, qui cherche à améliorer notre compréhension de la façon dont les corps détectent les virus. L’objectif à long terme de l’équipe est de traduire potentiellement ces résultats en traitements antiviraux qui peuvent lutter contre plusieurs virus.
Les modifications des protéines sont des molécules supplémentaires ou des groupes chimiques ajoutés à une protéine après sa réalisation. Les gènes fournissent des instructions pour créer des protéines molécule par molécule, mais la molécule n’est pas terminée une fois ce processus terminé.
Les enzymes cellulaires ajoutent ensuite de nouvelles pièces à la protéine pour les configurer pour certaines fonctions ou signaler la protéine pour la destruction. Ces modifications des protéines permettent à notre corps de réguler certains processus – ou de les arrêter complètement.
MDA5 est une protéine impliquée dans la toute première étape de la façon dont les corps humains détectent les virus. Il existe des sites spécifiques dans MDA5 où la modification des protéines se produit dans le cadre de la première étape de la réponse à un virus. Une petite protéine appelée ISG15 s’attache à ces sites – un processus appelé Isgylation, explique le premier auteur de l’étude, Lucky Sarkar, Ph.D., chercheur postdoctoral dans le laboratoire du Dr Gack.
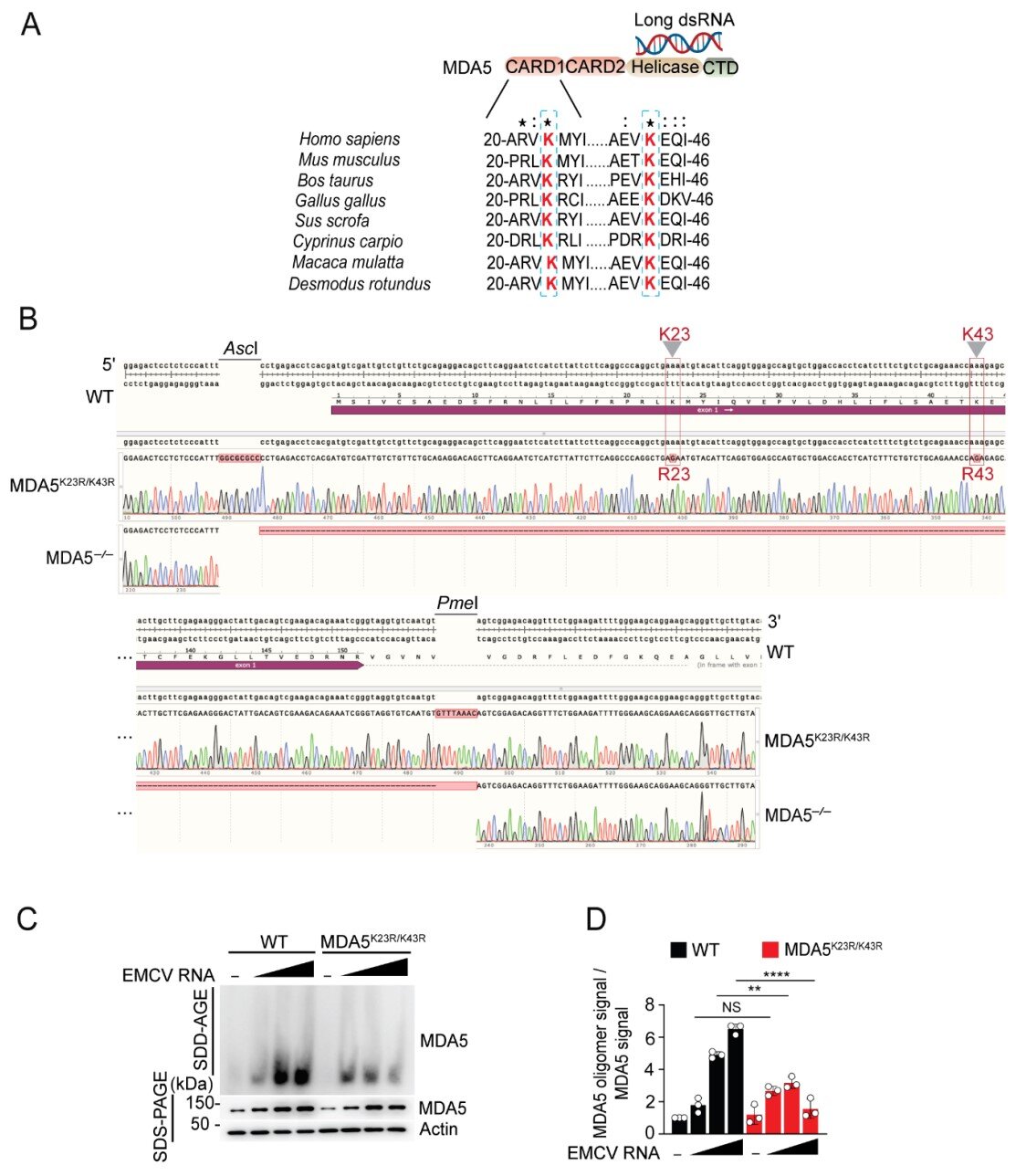
Pour explorer à quel point cette modification spécifique des protéines est critique à la détection des virus, les chercheurs ont travaillé avec la Case Western Reserve Transgenic and Cibunting Facility pour créer un modèle préclinique hébergeant une version de MDA5 qui manquait des sites nécessaires pour se fixer à ISG15.
« L’élimination de la capacité de la protéine à être modifiée avait presque le même effet que le supprimer complètement », a déclaré le Dr Sarkar. « Les données démontrent que la modification ISG15 de MDA5 est essentielle pour activer l’immunité innée – notre première ligne de défense de l’organisme. »
Sans Isgylation MDA5, les modèles précliniques d’infection par le virus de l’encéphalomyocardite (EMCV) étaient plus graves. La réplication virale et l’inflammation cardiaque ont augmenté de manière significative.
Des travaux antérieurs du laboratoire du Dr Gack ont montré que MDA5 sent de nombreuses autres familles de virus, notamment des coronavirus et des maladies transmises par les moustiques.
« Nous avons démontré que MDA5 utilise l’isgylation pour ressentir des envahisseurs viraux une fois qu’ils sont entrés dans notre corps », explique le Dr Gack. « L’isgylation MDA5 est un mécanisme pivot qui aide notre système immunitaire à répondre à un large éventail de virus. Comprendre ces processus fondamentaux derrière la façon dont le corps détecte un intrus est essentiel à la conception de traitements largement antiviraux. »
Drs. Gack et Sarkar disent que leurs résultats pourraient représenter la première étape pour développer un antiviral à large spectre. Les recherches actuelles sur la lutte contre les virus se concentrent principalement sur les vaccins spécifiques au virus ou les traitements antiviraux, explique le Dr Gack. Bien qu’il s’agisse d’excellents outils pour prévenir les infections spécifiques, elles sont faites sur mesure pour chaque virus ou même une seule souche d’un virus.
« À l’heure actuelle, nous demandons si nous pouvons moduler ces modifications de protéines pour augmenter notre réponse immunitaire innée naturelle pour le développement d’une approche largement antivirale pour plusieurs infections virales », explique le Dr Gack. « Ce serait un changement de jeu pour les nouveaux agents pathogènes et pour les situations où les approches traditionnelles ont échoué. »