Le trouble d’utilisation des opioïdes est associé à plus de 350 000 décès par an dans le monde. Guidés par la nécessité d’une compréhension accrue des caractéristiques neurobiologiques critiques de la dépendance, les chercheurs ont maintenant trouvé une signature moléculaire unique et des gènes dans le cortex orbitofrontal associé à un comportement de recherche d’héroïne.
Un modèle préclinique de rongeurs a impliqué un gène appelé Shisa7 comme prédicteur clé. Une nouvelle étude publiée dans Psychiatrie biologique Fournit des informations précieuses sur les mécanismes neurobiologiques qui sous-tendent la dépendance à l’héroïne et peuvent avoir des implications pour le développement de stratégies innovantes pour lutter contre l’épidémie d’opioïdes en cours.
L’enquêteur principal Yasmin L. Hurd, Ph.D., Départements de neurosciences et de psychiatrie, Friedman Brain Institute, ICAHN School of Medicine du Mount Sinai et Addiction Institute of Mount Sinaï, New York, « Mon équipe de recherche et moi sommes amenés à étendre les perspicaces neurobiologiques sous-jacentes à la dépendance.
« En examinant les signatures moléculaires dans le cerveau des utilisateurs d’opioïdes humains, nous espérons mieux comprendre la neuropathologie du trouble de la consommation d’opioïdes au-delà des mécanismes de récompense aigus et d’identifier de nouvelles voies de traitement pertinentes pour les phénotypes centraux qui perpétuent la consommation de substances. »
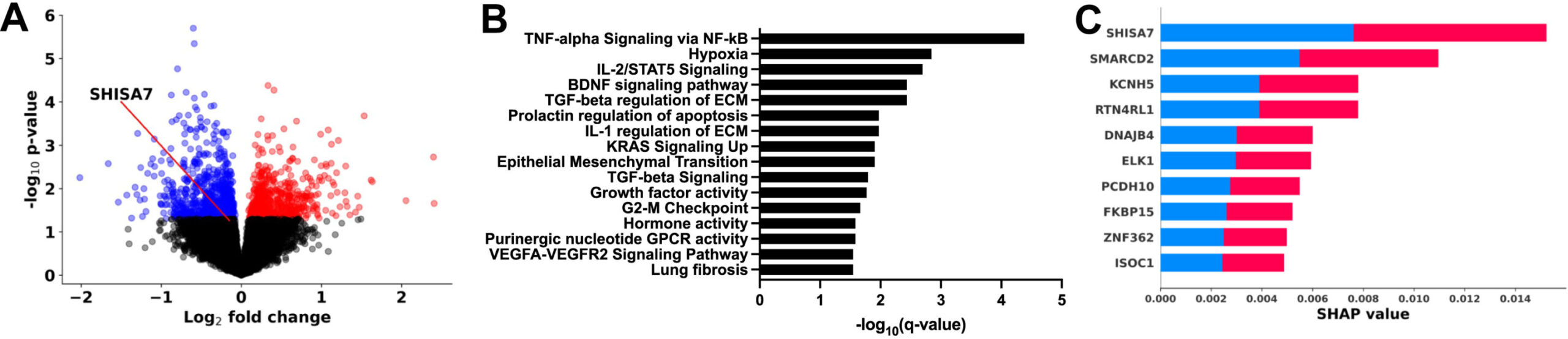
Dans cette étude, l’équipe de recherche a appliqué l’apprentissage automatique pour distinguer la signature moléculaire dans le cortex orbitofrontal, une région du cerveau critique pour les aspects du contrôle des impulsions, le comportement de recherche de médicaments et les fonctions cognitives liées aux troubles de la consommation de substances.
Les enquêteurs ont constaté que l’algorithme d’apprentissage automatique n’était pas seulement efficace pour identifier les signatures distinguant le cerveau d’un utilisateur d’héroïne humain, mais il a également identifié le gène le plus prédictif de cette signature moléculaire appelée Shisa7 qui n’avait pas été explorée précédemment dans le domaine. Une enquête plus approfondie a révélé que la modulation de l’expression de ce gène dans le cortex orbitofrontal influence le comportement de recherche d’héroïne et la flexibilité cognitive.
Le Dr Hurd ajoute: « Nous avons également observé que lorsque nous avons surexprimé SHISA7 chez les animaux naïfs de médicaments, il a complètement issu la signature du transcriptome observée avec une utilisation répétée de l’héroïne. Fait intéressant, la signature de Shisa7 liée à une maladie neurodégénérative et aux processus neuro-immunes.
« De plus, nous avons déterminé que les protéines qui se lient à SHISA7 étaient liées à la fois au GABA (le neurotransmetteur inhibiteur primaire dans le système nerveux central des mammifères) et au glutamate (le primaire des neurotransmetteurs excitateurs dans les voies de la maladie neurodégénaire centrale). »
L’auteur principal de l’étude Randall Ellis, Ph.D., Department of Neuroscience and Department of Psychiatry, Friedman Brain Institute, Icahn School of Medicine at Mount Sinai, et Addiction Institute of Mount Sinai, New York, qui met en évidence le potentiel de notre approche de l’apprentissage automatique avancé.
« L’application de l’apprentissage automatique de cette manière est exceptionnellement utile pour mieux comprendre les ensembles de données à haute dimension, tels que les milliers de gènes capturés par le séquençage d’ARN, pour découvrir de nouveaux modèles dans l’expression des gènes qui peuvent prédire efficacement les états pathologiques.
« Cette stratégie dans la mise à profit des données des utilisateurs d’opioïdes humains est particulièrement importante car nous recherchons des stratégies innovantes pour lutter contre l’épidémie d’opioïdes en cours. De plus, nos résultats mettent en évidence les risques potentiels à long terme de l’utilisation d’opioïdes pour les maladies neurodégénératives futures. »
John Krystal, MD, rédacteur en chef de Biological Psychiatry, a déclaré: « Cette étude met en évidence la biologie complexe du trouble de la consommation d’opioïdes. Des études minutieuses des tissus cérébraux post-mortem, en utilisant des analyses guidées par l’IA, sont essentielles pour identifier les éléments de construction moléculaire de la toxicomanie. Il est intéressant qu’une cible identifiée dans ce processus, soit également une augmentation des animaux.
Le Dr Hurd conclut: « Ces résultats de translation mettent en évidence l’importance d’étudier le cerveau humain, qui peut aider à découvrir de nouveaux systèmes biologiques sous-jacents au trouble qui pourrait finalement ouvrir de nouvelles avenues de traitement. »