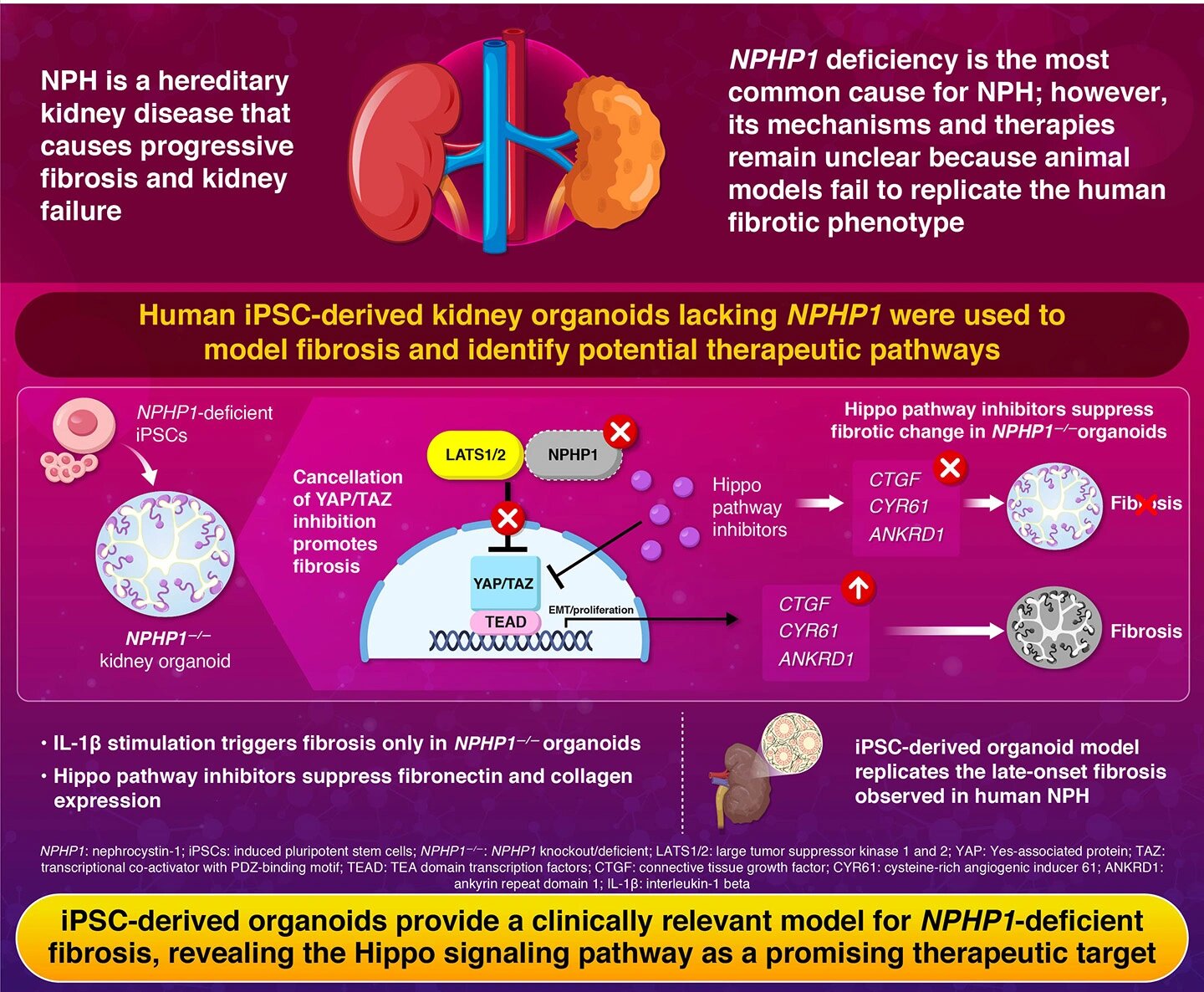
En utilisant des organoïdes rénaux dérivés de cellules souches pluripotentes induites par l’homme, des chercheurs de Science Tokyo ont découvert comment une signalisation anormale d’Hippo entraîne la fibrose dans la néphronophtise, une maladie rénale génétique causée par un déficit en NPHP1.
Leurs conclusions publiées dans Recherche et thérapie sur les cellules souches, démontrent que l’inhibition de la voie de signalisation Hippo supprime efficacement la fibrose du tissu rénal. L’étude met en valeur le potentiel des modèles de maladies basés sur les organoïdes pour élucider les mécanismes de la maladie tout en offrant une nouvelle cible thérapeutique pour la néphronophtise.
Comprendre la néphronophtise et ses enjeux
La néphronophtise (NPHP) est une maladie rénale héréditaire caractérisée par une fibrose progressive du rein, qui implique une accumulation anormale de tissus cicatriciels dans le rein. C’est l’une des principales causes d’insuffisance rénale terminale chez les enfants et les jeunes adultes, représentant environ 10 % de tous les cas de dialyse pédiatrique.
Malgré des décennies de recherche, il n’existe à ce jour aucun traitement efficace contre le NPHP, à l’exception de la transplantation rénale.
La maladie résulte généralement de mutations ou de délétions du gène NPHP1, qui fournit des instructions pour fabriquer la protéine néphrocystine-1, essentielle au maintien de tubules rénaux sains. Cependant, le mécanisme exact sous-jacent à la maladie reste flou car les modèles animaux appropriés du NPHP1 lié à NPHP1 ne parviennent pas à reproduire les changements fibrotiques sévères observés chez les patients humains.
Développer un modèle organoïde rénal basé sur l’humain
Pour surmonter ce défi de longue date, une équipe de recherche dirigée par le professeur agrégé Eisei Sohara, ainsi que par le professeur agrégé junior Koichiro Susa et l’étudiant diplômé Takefumi Suzuki du Département de néphrologie, École supérieure des sciences médicales et dentaires, Institut des sciences de Tokyo (Science Tokyo), a développé un modèle organoïde rénal humain utilisant des cellules souches pluripotentes induites par l’homme (iPS).
« Pour modéliser le déficit en NPHP1 observé dans la néphronophtise, nous avons utilisé l’édition du génome pour supprimer le gène NPHP1 », explique l’auteur principal Sohara. « De cette façon, nous avons généré des lignées cellulaires iPS déficientes en NPHP1 qui se sont ensuite différenciées en organoïdes rénaux tridimensionnels. » Ces mini structures rénales auto-organisées pourraient imiter avec précision l’architecture et la composition cellulaire du néphron humain.
Lorsque ces organoïdes rénaux déficients en NPHP1 ont été exposés à de faibles niveaux de signaux inflammatoires (interleukine-1β), ils ont présenté des changements fibrotiques frappants qui n’ont pas été observés dans les organoïdes rénaux normaux.
Des analyses microscopiques et moléculaires détaillées ont révélé une surexpression de gènes liés à la fibrose tels que la fibronectine, le collagène et le CTGF, indiquant l’activation d’une voie clé de signalisation de la fibrose dans les organoïdes déficients en NPHP1.
Le rôle de la voie de signalisation hippopotame dans la fibrose
Une enquête plus approfondie a révélé une activation anormale de la voie de signalisation Hippo dans les organoïdes déficients en NPHP1. La voie de signalisation Hippo est un réseau moléculaire qui régule la croissance et la réparation des tissus, aidant ainsi à prévenir les cicatrices excessives en contrôlant l’activité des protéines YAP et TAZ, les activateurs centraux de cette voie. L’absence de NPHP1 perturbe cette régulation, conduisant à une signalisation fibrotique incontrôlée.
« Nos résultats révèlent que NPHP1 interagit avec les composants de la voie Hippo pour maintenir un équilibre entre réparation et fibrose », explique Sohara. « Lorsque cette interaction est perdue, la voie Hippo devient hyperactive, entraînant des lésions rénales progressives. »
Tester des thérapies et des orientations futures
Pour explorer le potentiel thérapeutique du blocage de cette voie, l’équipe a testé plusieurs inhibiteurs de la voie Hippo sur le modèle organoïde. Parmi eux, la vertéporfine, un médicament activé par la lumière déjà approuvé pour traiter une maladie oculaire courante appelée dégénérescence maculaire, a également été testée. De manière frappante, la vertéporfine a efficacement inversé les marqueurs de la fibrose et a également réduit l’accumulation de gènes liés à la fibrose.
« La vertéporfine étant déjà utilisée en clinique, elle offre une option de traitement immédiate pour la néphronophtisie », note Susa.
Dans l’ensemble, la recherche marque une étape majeure vers la traduction de la recherche sur les cellules souches en thérapies pratiques pour les maladies rénales rares.
En tant que première étude à tester avec succès des médicaments sur un modèle NPHP humain dérivé d’iPSC, elle démontre comment les technologies organoïdes peuvent remplacer les modèles animaux pour une modélisation plus précise des maladies et des tests de médicaments personnalisés.
À l’avenir, les chercheurs prévoient d’améliorer leur plateforme organoïde rénale pour étudier des voies de signalisation supplémentaires et tester davantage de médicaments candidats contre la fibrose rénale, ouvrant ainsi la voie à des traitements plus sûrs et plus efficaces contre les maladies rénales chroniques.