Un groupe de recherche collaboratif a développé un nouveau candidat thérapeutique susceptible d’améliorer le pronostic des effets indésirables cutanés graves tels que le syndrome de Stevens-Johnson (SJS) et la nécrolyse épidermique toxique (TEN).
Les SJS/TEN sont des maladies graves avec un taux de mortalité élevé d’environ 30 %. Le groupe de recherche a précédemment révélé qu’un type de mort cellulaire programmée connue sous le nom de nécroptose, médiée par le récepteur 1 du formyl peptide (FPR1), se produit dans la peau lésionnelle des patients SJS/TEN.
Dans cette étude, l’équipe, dirigée par Haruna Kimura (étudiant diplômé), le professeur Takemasa Ozawa du Département de chimie de l’École des sciences de l’Université de Tokyo, et d’autres, a développé un inhibiteur qui supprime la nécroptose, démontrant qu’il réduit efficacement la mort cellulaire dans les cellules modèles SJS/TEN et empêche l’apparition de la maladie chez les souris modèles.
Les résultats ont été publiés dans Communications naturelles.
Les SJS/TEN sont déclenchés par l’administration de médicaments et caractérisés par une érosion de la peau et des muqueuses. Selon les directives cliniques japonaises, les corticostéroïdes systémiques constituent le traitement de première intention et, dans les cas réfractaires, une thérapie par immunoglobuline intraveineuse ou par échange plasmatique est utilisée. Cependant, environ 30 % des patients souffrent encore d’issues fatales, ce qui souligne le besoin urgent de nouvelles options thérapeutiques plus efficaces.
Le groupe de recherche a précédemment découvert que la nécroptose se produit dans les kératinocytes au sein des lésions SJS/TEN et que ce processus est induit par la stimulation de FPR1, un récepteur exprimé sur les cellules épidermiques. Dans cette étude, l’équipe a développé un système de criblage pour identifier les composés ayant une forte activité inhibitrice de FPR1 et a utilisé des cellules modèles SJS/TEN pour démontrer l’efficacité potentielle des inhibiteurs de FPR1 en tant qu’agents thérapeutiques nouveaux.
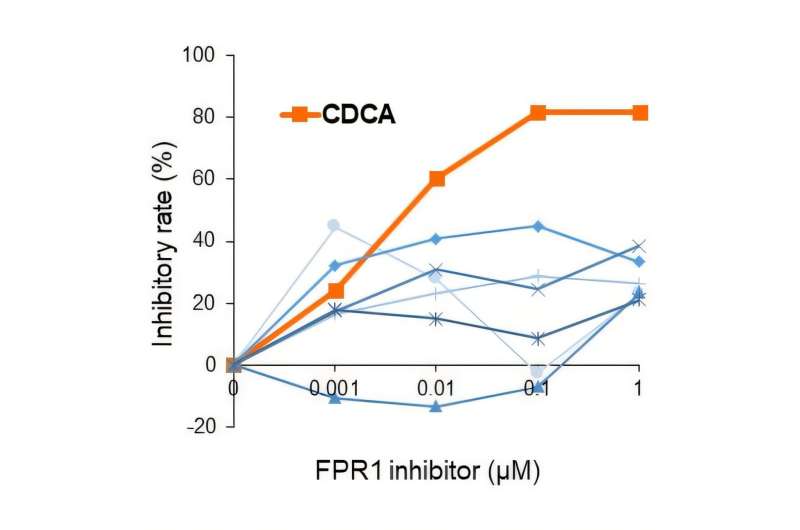
L’équipe a recherché des inhibiteurs puissants de FPR1 à l’aide de la bibliothèque de composés de la Drug Discovery Initiative de l’Université de Tokyo. FPR1 appartient à une famille de récepteurs connus sous le nom de récepteurs couplés aux protéines G (GPCR), qui fonctionnent via des voies de signalisation médiées par les protéines G et les β-arrestines.
Le groupe du professeur Ozawa avait précédemment développé des tests de protéines G et de β-arrestine capables de détecter chaque voie de signalisation indépendamment. À l’aide de ces tests, les chercheurs ont examiné la bibliothèque de composés de l’Université de Tokyo et sélectionné deux composés candidats présentant une activité inhibitrice élevée de FPR1. De plus, cinq autres composés précédemment signalés comme inhibant FPR1 ont été inclus comme candidats de référence.

