La sclérose en plaques (SEP) est une maladie auto-immune chronique qui touche plus de 2,9 millions de personnes dans le monde. Cela se produit lorsque le système immunitaire attaque par erreur la gaine de myéline, l’isolation protectrice autour des fibres nerveuses, provoquant une perturbation des signaux nerveux entre le cerveau et le corps. Les symptômes peuvent inclure des engourdissements, des picotements, une perte de vision et une paralysie.
Bien que les traitements actuels puissent réduire l’inflammation, il n’existe pas encore de thérapie pour protéger les neurones ou restaurer la gaine de myéline endommagée. Les chercheurs ont désormais franchi une étape majeure dans le développement d’une telle thérapie. Ils ont identifié deux composés susceptibles de remyéliniser les axones endommagés.
Publié dans la revue Rapports scientifiquesla recherche a été dirigée par Seema Tiwari-Woodruff, professeur de sciences biomédicales à la faculté de médecine de l’Université de Californie à Riverside, et John Katzenellenbogen, professeur de chimie à l’Université de l’Illinois à Urbana-Champaign.
« Notre travail représente plus d’une décennie de collaboration, les quatre dernières années étant axées sur l’identification et l’optimisation de nouveaux médicaments candidats présentant un fort potentiel pour traiter la SEP et éventuellement d’autres maladies neurologiques impliquant une démyélinisation », a déclaré Tiwari-Woodruff.
Les chercheurs ont pu lancer un programme autorisé par Cadenza Bio, Inc. La société progresse désormais vers l’évaluation clinique en tant que traitement potentiel de première classe pour les personnes vivant avec la SEP.
De la découverte au développement
Le projet s’appuie sur des recherches antérieures impliquant un composé appelé chlorure d’indazole, connu pour favoriser la remyélinisation et moduler le système immunitaire dans des modèles murins de SEP. Bien qu’efficace, le chlorure d’indazole ne possédait pas les propriétés pharmacologiques et la brevetabilité nécessaires au développement clinique et aux investissements commerciaux, a déclaré Tiwari-Woodruff.
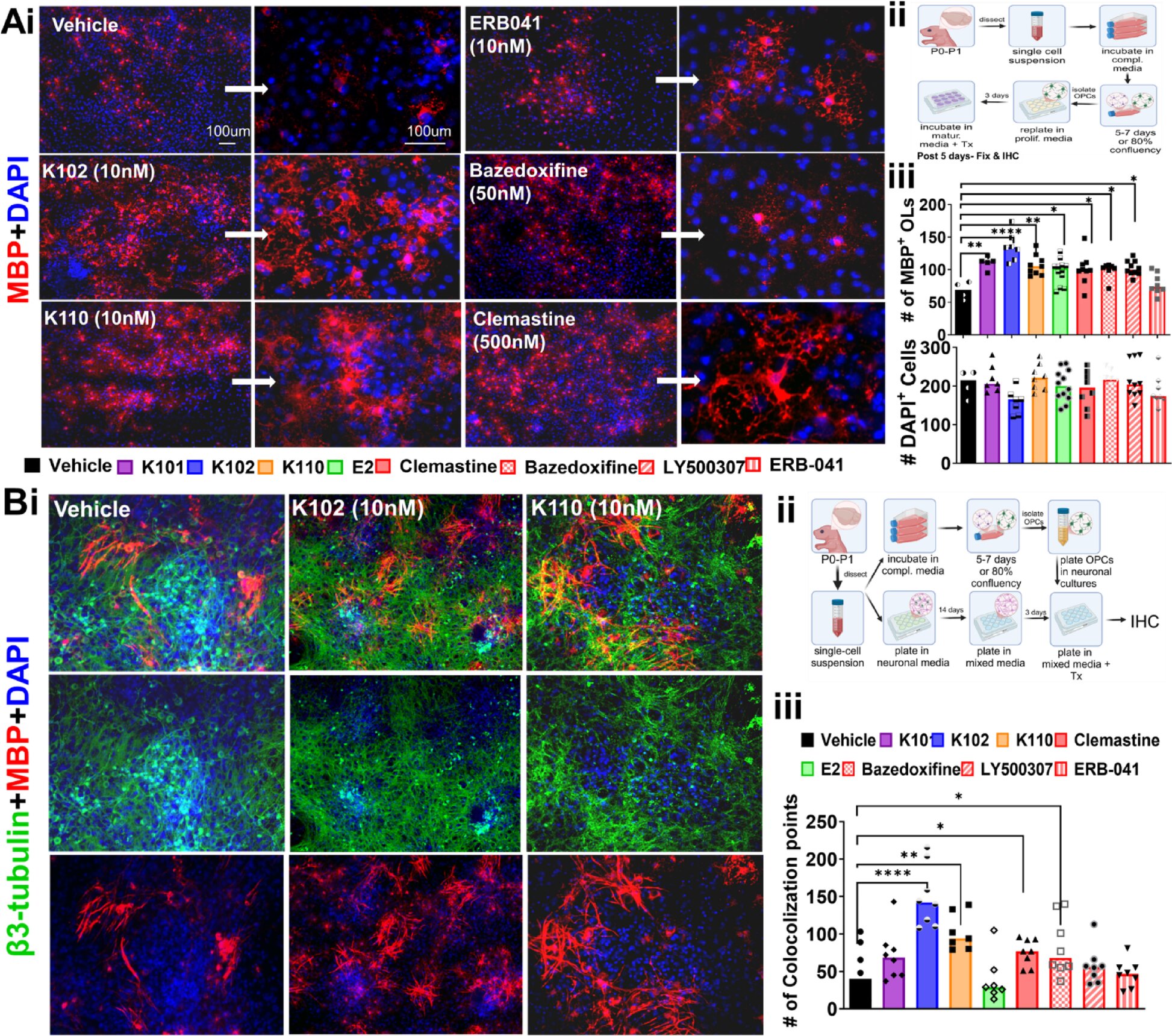
En collaboration avec les chimistes de l’UIUC Katzenellenbogen et Sung Hoon Kim, qui ont synthétisé les composés, le groupe de recherche de Tiwari-Woodruff, dirigé par Micah Feri, récemment diplômé de l’UCR, a examiné plus de 60 analogues du chlorure d’indazole. Cette collaboration a identifié deux candidats principaux, K102 et K110, qui présentaient une sécurité, une efficacité et des propriétés médicamenteuses améliorées dans les modèles murins et dans les cellules humaines.
Parmi les deux, le K102 est apparu comme le composé leader. Les chercheurs ont découvert qu’il favorise non seulement la remyélinisation, mais module également la fonction immunitaire, un équilibre important pour les traitements contre la SEP. Elle a également montré des résultats prometteurs sur les oligodendrocytes humains, les cellules myélinisantes du système nerveux central, dérivées de cellules souches pluripotentes induites, suggérant le potentiel de traductibilité entre les modèles animaux et la maladie humaine.
Dans des conditions normales, les cellules précurseurs des oligodendrocytes se transforment en oligodendrocytes producteurs de myéline pour réparer la myéline endommagée. Cependant, dans la SEP, ce processus naturel de réparation échoue souvent, entraînant des lésions nerveuses permanentes. Une remyélinisation réussie grâce à un composé comme le K102 pourrait restaurer une conduction nerveuse plus rapide et contribuer à réduire l’invalidité à long terme associée à la maladie.
« K110 est également un candidat sérieux », a déclaré Tiwari-Woodruff. « Il a des effets légèrement différents sur le système nerveux central et peut être mieux adapté à d’autres conditions comme les lésions de la moelle épinière ou les traumatismes crâniens, nous le gardons donc en préparation. »
Plus d’une décennie en préparation
Tiwari-Woodruff et Katzenellenbogen travaillent ensemble depuis plus de 12 ans. Bien que l’objectif initial soit la SEP, l’équipe pense que les K102 et K110 pourraient éventuellement être appliqués à d’autres maladies impliquant des lésions neuronales, notamment les accidents vasculaires cérébraux et la neurodégénérescence.
Cadenza Bio fait actuellement progresser le K102 dans le cadre des études non cliniques nécessaires pour soutenir les premiers essais cliniques chez l’homme.
« Nous espérons que les essais cliniques pourront bientôt commencer », a déclaré Tiwari-Woodruff. « Cela a été un long voyage, mais c’est là l’essence même de la science translationnelle : transformer la découverte en impact concret. »